Begrænset kendskab til effekten af vaccinationer og A-vitamintilskud på børnedødeligheden i Afrika
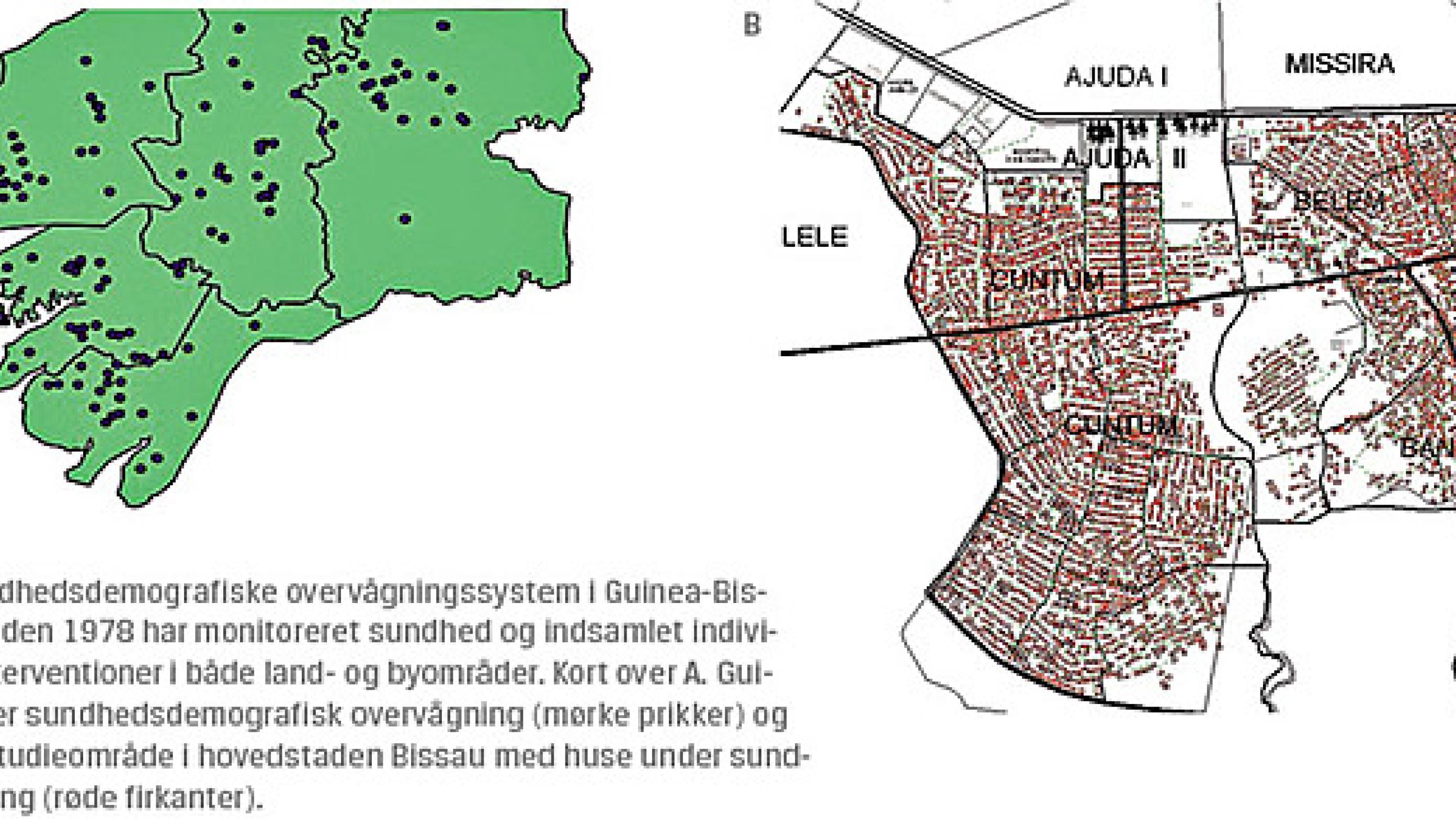

Ane Bærent Fisker1, 2, 3, Sanne Marie Thysen1, 2, 4, Christine Stabell Benn1, 2, 3 & Peter Aaby1, 2
WHO’s vaccinationsprogram, Expanded Programme on Immunizations (EPI), har siden 1970’erne forhindret millioner af dødsfald pga. mæslinger, difteri og pertussis. I det anbefalede vaccinationsprogram i lavindkomstlande er kernen bacille Calmette-Guérin (BCG)-vaccine og oral poliovaccine (OPV) ved fødslen, tre doser difteri-tetanus-pertussis (DTP)-vaccine og OPV tidligt i spædbarnsalderen samt en mæslingevaccine (MV) ved ni måneder (Figur 1). Men selvom programmet forhindrer både epidemier og dødsfald, er den reelle effekt ukendt. Viden om, hvilken effekt programmet har på det generelle sundheds- og dødelighedsniveau (den reelle effekt), er begrænset. Bandim Health Projects demografiske overvågning af en stor del af Guinea-Bissaus befolkning gennem de seneste 40 år har gjort det muligt at dokumentere, at de reelle effekter af vacciner og andre præventive sundhedsinterventioner ofte er meget anderledes end forventet. Det har derfor også været muligt at levere data, som kan bruges til at optimere vaccinationsprogrammet. Der er traditionelt blevet sat lighedstegn mellem vacciners forebyggende effekt på det specifikke patogen og deres effekt på den generelle sundhed. Således har man i WHO antaget, at vaccinernes samlede effekt kunne forudsiges på baggrund af den specifikke effekt og den estimerede sygdomsbyrde [1]; hvis for eksempel mæslingeinfektion forårsager 15% af dødsfaldene blandt børn, vaccinen er 90% effektiv, og vaccinationsdækningen er 85%, vil den forventede reduktion i dødeligheden ved at indføre en MV være 11% (0,90 × 0,85 × 0,15 = 0,11).
Virkeligheden er mere kompleks. Observationelle studier [2, 3] og randomiserede forsøg [4, 5] tyder på en langt større gavnlig effekt af MV; vaccinen sænker dødelighed og sygelighed ud over at forebygge mæslinger [4]. MV har med andre ord gavnlige uspecifikke
effekter. Der er også gavnlige uspecifikke effekter af
andre levende vacciner såsom BCG [6] og OPV [7].
I modsætning til de gavnlige uspecifikke effekter af de levende vacciner ses der ingen gavnlige uspecifikke effekter af de ikkelevende vacciner: På trods af beskyttelse mod målsygdommene tyder data på, at DTP øger dødeligheden for piger [8, 9].
Kontrasten mellem effekterne af de levende og de ikkelevende vacciner er konsistent: WHO gennemførte i 2013-2014 et litteraturreview af effekten af DTP, BCG og MV på dødeligheden blandt børn under fem år og fandt modsatrettede effekter af de levende vacciner mod tuberkulose (BCG) og mæslinger og den ikkelevende DTP-vaccine [2]. Mens de levende vacciner var forbundet med en næsten halvering af børnedødeligheden, var den inaktiverede DTP-vaccine forbundet med en tendens til højere dødelighed [2]. Kontrasten mellem de levende og de ikkelevende vacciner blev observeret i alle populationer, hvor begge typer vacciner blev undersøgt [2]. Det er vanskeligt at forestille sig en bias, som i den samme population kan være associeret med lavere dødelighed for MV og BCG, men med højere dødelighed for DTP [2, 8].
Vaccinerne, som anvendes i EPI, er ikke blevet undersøgt for deres effekt på generel børnedødelighed, før programmet blev rullet ud i 1970’erne. Da programmet implementeres i områder med sparsomme og usikre data til beskrivelse af dødeligheden, er effekterne blevet overset. Data fra de seneste 40 års monitorering af dødelighed og interventioner i Guinea-Bissau tyder på, at vi kunne anvende vaccinerne meget bedre, end vi gør: Et vaccinationsprogram, hvor man tilstræber, at barnet i længst mulig tid har fået en levende og ikke
en ikkelevende vaccine som den seneste, ville optimere
effekten.
I det nuværende vaccinationsprogram afsluttes spædbarnets vaccinesekvens med en MV ved ni måneder, men det antages, at enhver forsinket vaccine, der gives ved en senere kontakt, vil medføre bedre sundhed. Den nugældende anbefaling er, at manglende vaccinedoser skal gives ved en senere kontakt, uden hensyntagen til sekvensen [10].
Eftersom den sidst givne vaccine har den stærkeste uspecifikke effekt på barnets immunsystem, kan en ændring af vaccinesekvensen med en ikkelevende vaccine som den seneste imidlertid have den modsatte effekt. Adskillige studier tyder på, at DTP-indeholdende vacciner, der gives efter MV, øger dødeligheden. I metaanalysen af de tre studier, som indgik i WHO’s review [11-13], var dødeligheden 2,66 (95% konfidens-interval (KI): 1,04-6,81) gange højere for børn, der var vaccineret med DTP efter MV, end for børn, der var vaccineret med MV efter DTP [2]. De senere tilkomne studier [14, 15] viser samme billede: Dødeligheden er fortsat 2,11 (95% KI: 1,39-3,21) gange højere for børn, som har fået DTP som den seneste vaccine efter MV (Figur 2).
P.t. tages der ikke højde for uspecifikke effekter af vaccinerne i planlægningen eller evalueringen af vaccinationsprogrammet. Som hovedindikator for kvaliteten af de nationale EPI i lavindkomstlande anvendes dækningen med den tredje dosis af DTP-vaccinen (DTP3) i ved 12 måneder. I Global Vaccine Action Plan er målet at opnå national DTP3-dækning på 90%, og at dækningen i alle distrikter skal være over 80% [1]. Men at opnå disse mål vil næppe bedre børnesundheden. For at sikre, at effekten af vaccinationsprogrammet på børns sundhed optimeres, burde man i stedet specificere, at alle børn skulle vaccineres tidligt med de levende BCG-vacciner og MV, og at alle børn skulle afslutte deres vaccinationssekvens med en levende MV efter DTP3.
Men fokus er andetsteds. Vi har i Guinea-Bissau
observeret, at MV-dækningen på trods af en øget investering i at levere vacciner er faldet. I 2008 blev den trivalente DTP-vaccine erstattet af den pentavalente DTP-HIB-hepatitis B-vaccine, som var betydeligt dyrere. Vaccinationsprogrammet fik tilført flere ressourcer, og vi kunne måle, at dækningen af den DTP-indeholdende vaccine steg [16], og at de ekstra ressourcer medførte, at de pentavalente vacciner blev givet tættere på det anbefalede vaccinationstidspunkt. Men på trods af de hyppigere kontakter blev MV givet senere, og dækningen faldt [16] (Tabel 1). De modsatrettede effekter af MV og DTP skyldes, at der samtidig var øget fokus på vaccinespild: Den levende MV leveres i tidosishætteglas, som skal anvendes inden for seks timer efter åbning. Dette har medført, at et MV-hætteglas ikke åbnes, medmindre seks børn skal vaccineres. Vi har registreret, at mødrene ofte går forgæves med deres børn [17]. Således har man, for at spare på vaccinen, spildt vaccinationschancer og øget omkostninger for familierne, som skal bringe deres børn til vaccination flere gange [17], og for sundhedssystemet, som må afholde flere vaccinationssessioner og behandle flere syge børn [18].
Et fokus på vaccinespild er også medvirkende til, at BCG-vaccinens potentiale til at bedre spædbørns overlevelse ikke udnyttes optimalt. BCG-vaccinen leveres
ligesom MV i multidosishætteglas og skal anvendes inden for seks timer efter åbning, hvilket har medført, at en stor del af børnene ikke bliver vaccineret ved første kontakt med sundhedssystemet [19]. Medianalderen for BCG-vaccination er over en måned, selvom vaccinationen anbefales foretaget ved fødslen, og vi har påvist, at mange kontakter ikke udnyttes til vaccination [19].
Mens nogle interventioner, herunder vacciner, anbefales uden studier af effekten på den generelle dødelighed, blev effekten af højdosis-A-vitamin på dødelighed undersøgt i 1980-1990’erne. I en metaanalyse af otte randomiserede forsøg af A-vitamin versus placebo i 1993, fandt man en 23% reduktion i den generelle børnedødelighed ved tilskud af A-vitamin [20], og WHO anbefalede derfor at give A-vitamin hver 4.-6. måned i områder med høj dødelighed. Mekanismen bag effekten var dårligt forstået, og den gavnlige effekt, som sås i seks ud af otte studier, kunne ikke forklares med børnenes A-vitaminstatus [20, 21].
Med henblik på at forstå variationen og forbedre anvendelsen af A-vitamintilskud har vi ved Bandim Health Project undersøgt effekten af A-vitamintilskud både i kampagner og sammen med andre interventioner. Vi har studeret de parametre, der afgør, om A-vitamin er gavnligt eller skadeligt, og har fundet, at A-vitamin givet sammen med eller tæt på den levende MV lader til at være gavnligt [22, 23], mens A-vitamin givet sammen med eller tæt på den ikkelevende DTP-vaccine er forbundet med øget dødelighed [22-24].
I en reanalyse af et af de studier, som dannede baggrund for politikken om at give generelt A-vitamintil-skud, var hele den gavnlige effekt blandt ikkevaccinerede børn, mens der sås stærke negative effekter af A-vitamintilskud hos piger, som fik DTP-vaccine under opfølgningen [25]. Interaktioner mellem højdosis-A-vitamin og rutinevacciner kan således forklare, at der ikke lader til at være samme gavnlige effekt af A-vitamintil-skud i dag, som sås, da politikken blev formuleret [26]. Ved en kontinuerlig monitorering af interventioners effekt på børnesundheden kan man således identificere interaktioner mellem interventioner og derigennem være i stand til at optimere programmerne.
For ti år siden klassificererede Copenhagen Consensus højdosis-A-vitamin som en af verdens mest omkostningseffektive interventioner til reduktion af børnedødelighed [27]. Omkostningerne, der er forbundet med at levere A-vitamintilskud til 200 mio. børn hver 4.-6. måned, er dog betydelige. Man tænkte derfor, at ressourcerne kunne udnyttes bedre, hvis andre kontakter med sundhedssystemet blev anvendt til at give A-vitamin. Dette var hensigten med at anbefale, at eksisterende kontakter gennem vaccinationsprogrammet skulle anvendes til at levere A-vitamintilskud. Effekten af denne anbefaling blev ikke evalueret.
I 2007-2011, efter at A-vitamintilskud ved vaccinationskontakter efter seksmånedersalderen havde været anbefalet i > 15 år, undersøgte vi effekten af at give A-vitamin ved vaccinationskontakter. Blandt 7.587 børn, hvoraf to tredjedele fik A-vitamin eller placebo sammen med MV eller MV + DTP, fandt vi ikke nogen samlet gavnlig effekt. A-vitamin givet ved vaccinationskontakter var forbundet med øget dødelighed for drenge og lavere dødelighed for piger [28] (Figur 3). Anbefalingen om at give A-vitamintilskud sammen med vacciner kan således have været skadelig for drenge, uden at det er blevet undersøgt. Sådan forholder det sig desværre med mange sundhedsinterventioner: Anbefalinger laves på baggrund af undersøgelser af specifikke effekter i en bestemt kontekst. Man undersøger ikke, om effekten ændres, når andre parametre ændres.
P.t. er det samme A-vitamin- og vaccinationsprogram anbefalet til begge køn, men de uspecifikke effekter varierer med køn: Piger har den største gavnlige uspecifikke effekt af MV [2, 4, 16], men også den største negative effekt af DTP [9]. Drenge har derimod en mere gavnlig effekt af OPV end piger [7, 29].
A-vitamin er gavnlig for piger, når det bliver givet sammen med levende vacciner, skadelig, når det bliver givet sammen med ikkelevende vacciner, og skadelig for drenge når det bliver givet sammen med en kombination af levende og ikkelevende vacciner. At effekterne er forskellige for drenge og piger har vigtige implikationer, både for fremtidige vaccinationspolitikker (som kunne være forskellige for drenge og piger) og i evalueringen af vaccinationsprogrammer, da ændringer af pige-dreng-dødelighedsrater ved ændringer i programmet kan være et udtryk for uspecifikke effekter.
Antagelser om mekanismer og effekter frem for reelle data har præget de sundhedsfremmende interventioner i lavindkomstlandene. I lavindkomstlande med høj børnedødelighed er der et stort potentiale for at gøre en positiv forskel.
Men vi må ikke glemme, at vores interventioner ikke virker i et isoleret system, men i et komplekst immunsystem, hvor vi kan gøre både gavn og skade. Derfor bør vi udnytte de muligheder, der er, for at evaluere den reelle, samlede effekt af interventioner, som forventes at have gavnlige effekter på den generelle sundhed. Bandim Health Project har i de seneste 40 år undersøgt de reelle effekter af interventioner i Guinea-Bissau, og fundene viser, at enhver ny intervention bør ledsages af en monitorering af effekten på den generelle sundhed og for begge køn.
Korrespondance: Ane Bærent Fisker. E-mail: abf@ssi.dk
Antaget: 29. august 2018
Publiceret på Ugeskriftet.dk: 29. oktober 2018
Interessekonflikter: ingen. Forfatternes ICMJE-formularer er tilgængelige sammen med artiklen på Ugeskriftet.dk
Ane Bærent Fisker, Sanne Marie Thysen, Christine Stabell Benn & Peter Aaby:
Limited knowledge of the effect on child mortality of vaccinations and vitamin A supplementation
Ugeskr Læger 2018;180:V06180465
Preventive health interventions, including the vaccination and vitamin A supplementation programmes, are implemented in low-income countries with little assessment of the real-life effects on child mortality. Nevertheless, the programmes are frequently credited with large, finite numbers of deaths prevented. Forty years of demographic surveillance in Guinea-Bissau indicates, that vaccines and vitamin A supplementation have effects beyond what can be explained by preventing the target infections and vitamin A deficiency. Taking these effects into account would substantially improve child health.
World Health Organization. Global vaccine action plan 2011-2020. www.who.int/immunization/global_vaccine_action_plan/GVAP_doc_2011_2020/en/index.html (14. aug 2018).
Higgins JP, Soares-Weiser K, Lopez-Lopez JA et al. Association of BCG, DTP, and measles containing vaccines with childhood mortality: systematic review. BMJ 2016;355:i5170.
Kristensen I, Aaby P, Jensen H. Routine vaccinations and child survival: follow up study in Guinea-Bissau, West Africa. BMJ 2000;321:1435-8.
Aaby P, Martins CL, Garly ML et al. Non-specific effects of standard measles vaccine at 4.5 and 9 months of age on childhood mortality: randomised controlled trial. BMJ 2010;341:c6495.
Aaby P, Garly ML, Bale C et al. Survival of previously measles-vaccinated and measles-unvaccinated children in an emergency situation: an unplanned study. Pediatr Infect Dis J 2003;22:798-805.
Biering-Sørensen S, Aaby P, Lund N et al. Early BCG-Denmark and neonatal mortality among infants weighing <2500 g: a randomized controlled trial. Clin Infect Dis 2017;65:1183-90.
Lund N, Andersen A, Hansen AS et al. The effect of oral polio vaccine at birth on infant mortality: a randomized trial. Clin Infect Dis 2015;61:1504-11.
Aaby P, Ravn H, Benn CS. The WHO review of the possible non-specific effects of diphtheria-tetanus-pertussis vaccine. Pediatr Infect Dis J 2016;35:1247-57.
Aaby P, Ravn H, Fisker AB et al. Is diphtheria-tetanus-pertussis (DTP) associated with increased female mortality? Trans R Soc Trop Med Hyg 2016;110:570-81.
World Health Organisation. WHO recommendations for routine immunization – summary tables: interrupted and delayed vaccination. www.who.int/immunization/policy/Immunization_routine_table3.pdf (20. maj 2018).
Aaby P, Biai S, Veirum JE et al. DTP with or after measles vaccination is associated with increased in-hospital mortality in Guinea-Bissau. Vaccine 2007;25:1265-9.
Hirve S, Bavdekar A, Juvekar S et al. Non-specific and sex-differential effects of vaccinations on child survival in rural western India. Vaccine 2012;30:7300-8.
Aaby P, Nielsen J, Benn CS et al. Sex-differential and non-specific effects of routine vaccinations in a rural area with low vaccination coverage: an observational study from Senegal. Trans R Soc Trop Med Hyg 2015;109:77-84.
Welaga P, Oduro A, Debpuur C et al. Fewer out-of-sequence vaccinations and reduction of child mortality in Northern Ghana. Vaccine 2017;35:2496-503.
Fisker AB, Thysen SM. Non-live pentavalent vaccines after live
measles vaccine may increase mortality. Vaccine 2018;36:6039-42.
Fisker AB, Hornshoj L, Rodrigues A et al. Effects of the introduction of new vaccines in Guinea-Bissau on vaccine coverage, vaccine timeliness, and child survival: an observational study. Lancet Glob Health 2014;2:e478-87.
Byberg S, Fisker AB, Rodrigues A et al. Household experience and costs of seeking measles vaccination in rural Guinea-Bissau. Trop Med Int Health 2017;22:12-20.
Byberg S, Fisker AB, Thysen SM et al. Cost-effectiveness of providing measles vaccination to all children in Guinea-Bissau. Glob Health Action 2017;10:1329968.
Thysen SM, Byberg S, Pedersen M et al. BCG coverage and barriers to BCG vaccination in Guinea-Bissau: an observational study. BMC Public Health 2014;14:1037.
Beaton GH, Martorell R, McCabe G et al. Effectiveness of vitamin A supplementation in the control of young child morbidity and mortality in developing countries. United Nations Administrative Committee on Coordination/Sub-Committee on Nutrition, 1993.
Benn CS, Aaby P, Arts RJ et al. An enigma: why vitamin A supplementation does not always reduce mortality even though vitamin A deficiency is associated with increased mortality. Int J Epidemiol 2015;44:906-18.
Benn CS, Martins C, Rodrigues A et al. The effect of vitamin A supplementation administered with missing vaccines during national immunization days in Guinea-Bissau. Int J Epidemiol 2009;38:304-11.
Fisker AB, Aaby P, Bale C et al. Does the effect of vitamin A supplements depend on vaccination status? BMJ open 2012;2:e000448.
Benn CS, Rodrigues A, Yazdanbakhsh M et al. The effect of high-dose vitamin A supplementation administered with BCG vaccine at birth may be modified by subsequent DTP vaccination. Vaccine 2009;27:2891-8.
Benn CS, Aaby P, Nielsen J et al. Does vitamin A supplementation interact with routine vaccinations? Am J Clin Nutr 2009;90:629-39.
Benn CS, Fisker AB, Wieringa FT et al. Re: Vitamin A distribution in danger: Should we worry? Lancet 2018; 392: 631.
Horton S, Begin F, Greig A et al. Copenhagen Consensus: Micronutrient Supplements for Child Survival. https://www.copenhagenconsensus.com/publication/second-copenhagen-consensus-micronutrient-supplements-child-survival-best-practice (14. aug 2018).
Fisker AB, Bale C, Rodrigues A et al. High-dose vitamin A with vaccination after 6 months of age: a randomized trial. Pediatrics 2014;134:e739-e748.
Andersen A, Fisker AB, Rodrigues A et al. National immunization campaigns with oral polio vaccine reduce all-cause mortality: a natural experiment within seven randomized trials. Front Pub Health 2018;6:13.