Dermloop: kræftdiagnostik uden CE-mærket software
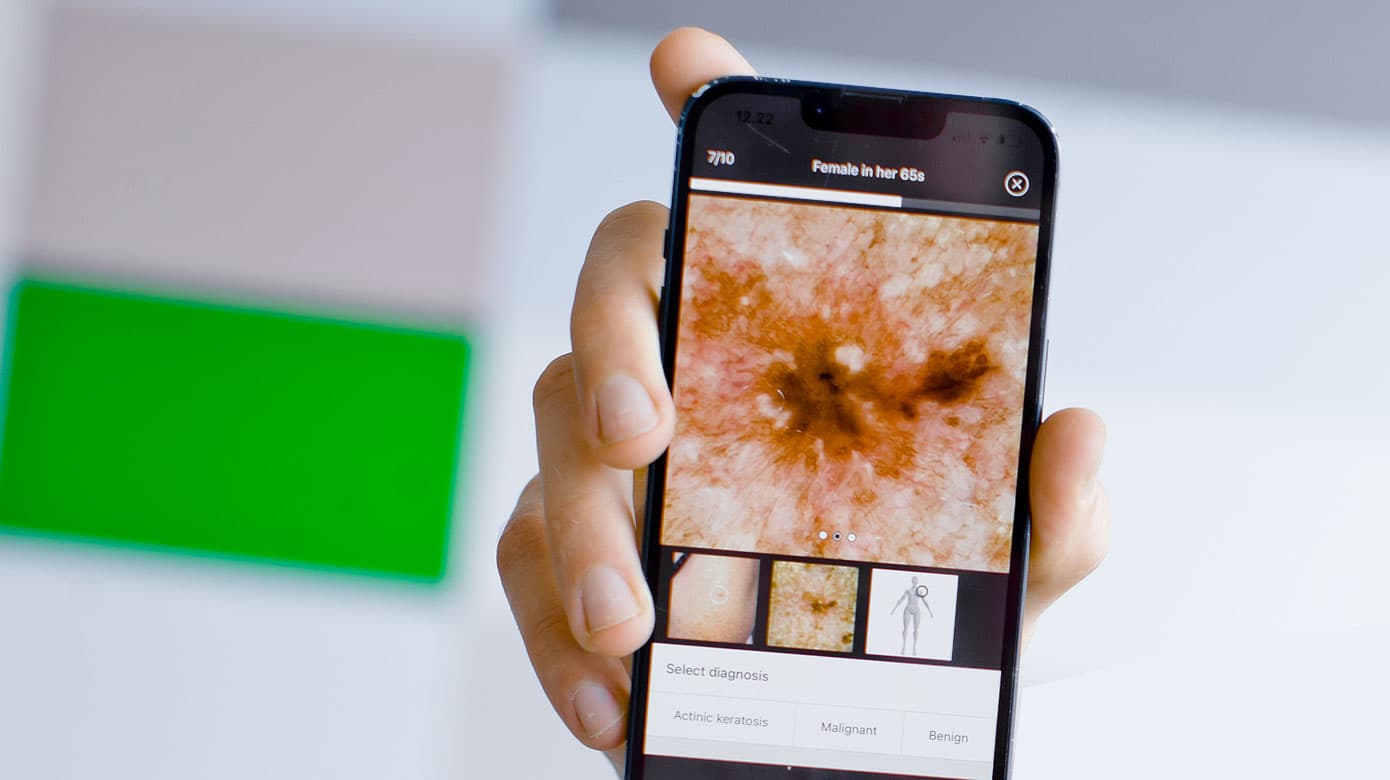

I almen praksis anvendes appen Dermloop til at tage dermatoskopiske billeder af hudlæsioner ved mistanke om hudkræft, som derefter sendes til vurdering hos hospitalsdermatologer. Den app, som via iPhone og en optisk dermatoskoplinse styrer billedoptagelsen og vurderer billedkvaliteten, er imidlertid ikke klassificeret som medicinsk udstyr og er derfor ikke CE-mærket.
CE-mærkning er et krav i forordningen om medicinsk udstyr (MDR) og sikrer, at udstyr er sikkert, fungerer som tilsigtet og er tilstrækkeligt dokumenteret. CE-mærkning er påkrævet for både medicinsk hardware og medicinsk software. Digital innovation i sundhedsvæsenet bør fremmes, men må ikke ske på bekostning af fornuftige krav til medicinsk udstyr.
Spørgsmålet er, om Dermloop forsvarligt kan undtages fra reglerne om medicinsk software. Det er relevant, fordi diagnostisk software risikoklassificeres bl.a. ud fra, om beslutninger baseret på softwaren kan medføre alvorlig helbredsforringelse eller død som ved malignt melanom.
Af databehandleraftalen indgået den 3. januar 2026 med producenten [1] fremgår det, at Dermloop er »en klinisk platform, der faciliterer vurdering og behandling af [...] patienter med hudtilstande«, og det fremgår også af databehandleraftalen, at systemet består af to stykker software: 1) Dermloop Capture, en iPhone-app, der sammen med et dermatoskop anvendes til at oprette og henvise sager til speciallæger, og 2) Dermloop Desktop, en webapplikation, hvor speciallæger vurderer sagerne og sender svar tilbage til henviser. Databehandleraftalen bidrager til forståelsen af det formål, som forudsættes og accepteres ved Dermloops faktiske anvendelse.
CE-mærkningspligten beror på producentens erklærede intended purpose, dvs. formålet angivet i produktmærkning, brugsvejledninger og markedsføring. Men hvis produktets funktionalitet åbenlyst tjener et medicinsk formål, bør producenten ikke kunne erklære et ikkemedicinsk formål og derved undgå CE-mærkning. Af producentens hjemmeside fremgik det den 14. januar 2026, at »Dermloop addresses skin lesion diagnostics« [2].
Dermloop udrulles aktuelt nationalt i projektsamarbejdet Digital Hudkræftdiagnostik. Region Hovedstaden er projektledende region.
Lægemiddelstyrelsen har tilkendegivet, at det alene er den optiske dermatoskoplinse, der skal CE-mærkes [3]. Linsen er imidlertid et passivt instrument og kan ikke i sig selv skabe diagnostiske billeder – billedoptagelsen sker via Dermloop Capture, der betjener smartphonekameraet. Spørgsmålet er derfor, om denne software bør betragtes som medicinsk udstyr.
Styrelsen beskriver Dermloop som »en telemedicinsk appløsning«, der er »udelukkende tiltænkt til overførsel af fotos fra et CE-mærket dermatoskop«, og som ikke »specifikt muliggør, at det medicinske udstyr (dermatoskopet) kan anvendes i overensstemmelse med sit erklærede formål« – og dermed ikke medicinsk udstyr [3]. Denne afgrænsning tager imidlertid ikke højde for, at Dermloop Capture også anvendes til selve billedoptagelsen og den tilhørende kvalitetssikring.
Dermatoskopet er CE-mærket som medicinsk udstyr i klasse I og svarer funktionelt til et passivt optisk hjælpemiddel til konventionel klinisk dermoskopi uden selvstændig digital billedbehandling. Af CE-erklæringen fremgår, at det erklærede formål er »skin lesions diagnosis«. Phone-adapteren, der alene fungerer som en mekanisk holder for den optiske linse på smartphonekameraet, beskrives som tilbehør, der muliggør »capture and display images«. Software er ikke nævnt i CE-erklæringen og er dermed ikke omfattet af denne.
Når appen tillige anvendes på en prækonfigureret smartphone med monteret dermatoskop og standardiseret arbejdsgang, tyder det på, at der er tale om et integreret klinisk system, og at softwaren ikke kan reduceres til blot at overføre fotos.
Den optiske linse anvendes sammen med Dermloop Capture-softwaren. Når et billede tages, betjener softwaren smartphonekameraet og anvender en algoritme til at vurdere billedkvaliteten, herunder om et billede bør tages om. Dermloop Capture bidrager dermed til kvalitetssikring af diagnostiske billeder. Softwaren indsamler også diagnostiske oplysninger om hudlæsionen, og der tages via Dermloop Capture også et oversigtsbillede af patientens hud uden påsat linse. Billeder af hudlæsioner, der oprettes i Dermloop Capture, gemmes hos producenten.
Ifølge MDR-artikel 2 [1] er software et medicinsk udstyr med tiltænkt anvendelse til diagnosticering, monitorering eller behandling, og MDR's tilhørende vejledning om medicinsk software MDCG 2019-11 præciserer, at software, der er tiltænkt at »process, analyse, interpret, calculate, create or modify medical information«, kan kvalificeres som medicinsk software, hvis dette sker med et »medicinsk formål«
Ifølge MDR Rule 11 klassificeres software, der er »intended to provide information which is used to take decisions with diagnosis or therapeutic purposes«, som minimum klasse IIa. Formuleringen forudsætter, at softwaren leverer information til beslutningstagning – ikke at softwaren selv træffer beslutninger.
Dermloop Capture muliggør, at der kan optages diagnostiske billeder med en passiv linse, hvis CE-erklærede formål er »skin lesions diagnosis«. App og linse er tiltænkt anvendt i funktionel sammenhæng, hvor softwaren ikke uden videre kan reduceres til overførsel af fotos.
Region Hovedstaden har i december 2025 bekræftet skriftligt, at der ikke findes dokumenter, som vurderer Dermloop Capture i forhold til MDR [4]. Region Hovedstadens MD-vurdering fra april 2024, som konkluderer, at »Dermloop ikke skal klassificeres som et medicinsk software« [5], vedrører således alene den overordnede platform, der »formidler workflowet mellem de involverede specialer«, og ikke den billedoptagende software.
MD-vurderingen angiver, at Dermloop er »et kommunikationsværktøj, der anvendes kun til formidling af data som billeder, anamnese og vurderinger, men ikke i sig selv anvendes til diagnostiske formål eller beslutningsstøtte«. Samme vurdering beskriver dog, at »når en klinisk bruger via Dermloop har taget et klinisk eller dermoskopisk billede, anvendes en algoritme til at vurdere, om billedet er uskarpt«, og bekræfter dermed, at billedet tages med softwaren.
Den tilhørende Data Protection Impact Assessment (DPIA) fra november 2025 anerkender risikoen for, at patienten modtager »en forkert vurdering og/eller behandling« med »meget alvorlige« konsekvenser, der kan »lede til et forkert forløb for patienten med eventuelle helbredsmæssige konsekvenser til følge« [5]. DPIA beskriver, at når »et billede tages, vil en algoritme vurdere, om billedet har en tilstrækkelig kvalitet eller bør tages om. I så fald advares brugeren herom og foreslås at tage et nyt billede«.
At disse risici fremgår, at en DPIA ikke ændrer ved deres relevans. For ifølge MDR Rule 11 skal software, der leverer information til diagnostiske beslutninger, som udgangspunkt klassificeres som minimum klasse IIa og som IIb eller III ved risiko for alvorlig helbredsskade eller død.
Lægemiddelstyrelsen har i juli 2025 oplyst, at deres vurdering af Dermloop ikke er en formel afgørelse og derfor ikke kan påklages [3]. Efter indgivelse af en anmeldelse vedrørende Dermloop Capture har Lægemiddelstyrelsen dog i korrespondance fra januar 2026 oplyst, at sagen nu genovervejes i dialog med producenten og styrelsens specialister. Der foreligger endnu ingen bindende afgørelse.
Når Dermloop anvendes i en risikokontekst med mistanke om kræft, bør der ikke herske tvivl om, hvilke komponenter der er medicinsk udstyr, og hvilke krav til dokumentation og sikkerhed der gælder. Det rimelige er ikke at opgive Dermloop eller standse innovation, men at der foretages en MDR-vurdering, hvor Dermloop Capture indgår som den centrale softwarekomponent i overensstemmelse med forordningens krav til medicinsk software.