3D-assisteret kirurgi ved rekonstruktion i hoved-hals-området

Lasse Østrup Petersen1, Birgitte Jul Kiil1, Søren Dührr Gade2, Anders Mølgaard Jakobsen3 & Andreas Engel Krag1, 4
3D-assisteret kirurgi har vundet indpas ved rekonstruktion af kæbeknogle.
Virtuel operationsplanlægning og 3D-printede skæreguider medfører præcise og patientspecifikke resultater.
3D-assisteret kirurgi er under fortsat udvikling, og bredere anvendelse forventes på tværs af kirurgiske specialer.
Rekonstruktion af underkæben er nødvendig efter tumorresektion, traumer eller osteoradionekrose, hvor et stykke af underkæben mangler. Rekonstruktionen bidrager til at bevare tyggefunktionen, beskytte de øvre luftveje og bevare et acceptabelt kosmetisk udseende [1, 2]. Underkæben kan rekonstrueres ved at flytte knogle fra andre steder på kroppen. Ved flytning af knogle genoprettes knoglens blodforsyning på recipientstedet ved karanastomoser foretaget under operationsmikroskop (såkaldt fri knoglelap). Den frie fibulaknoglelap er ofte førstevalg til sådanne rekonstruktioner af følgende årsager: god knoglekvalitet og -længde; mulighed for at medtage hud- og muskelvæv fra underbenet; minimal donorstedsmorbiditet, når de distale 6 cm mod ankelleddet bevares; og mulighed for dissektion af fibulalappen samtidig med resektionen af tumor i ansigtet [1, 3].
Traditionelt har man foretaget den partielle underkæberesektion og udskæring af et passende fibulasegment ved frihåndsteknik ud fra erfaring og øjemål med spejling af den kontralaterale underkæbeanatomi [4]. Hvor man tidligere især havde fokus på fibulalappens overlevelse, er der i dag øget fokus på at forbedre de funktionelle og æstetiske resultater ved rekonstruktion af underkæben [2]. Ved hjælp af 3D-assisteret kirurgi kan præoperative CT’er af underkæbe og fibula anvendes til virtuel planlægning af operationen samt 3D-printning af patientspecifikke modeller og skæreguider til udformning af den nye underkæbe [4].
Denne artikel omhandler konceptet 3D-assisteret kirurgi med udgangspunkt i rekonstruktion af underkæben ved operation for hoved-hals-kræft. Artiklen beskriver evidensen for 3D-assisteret kirurgi og diskuterer fordele og ulemper ved denne teknik sammenlignet med frihåndskirurgi. Artiklen belyser desuden muligheden for etablering af in-house 3D-centre samt fremtidsperspektiverne inden for 3D-assisteret kirurgi.
Præoperativ vurdering ved multidisciplinært team
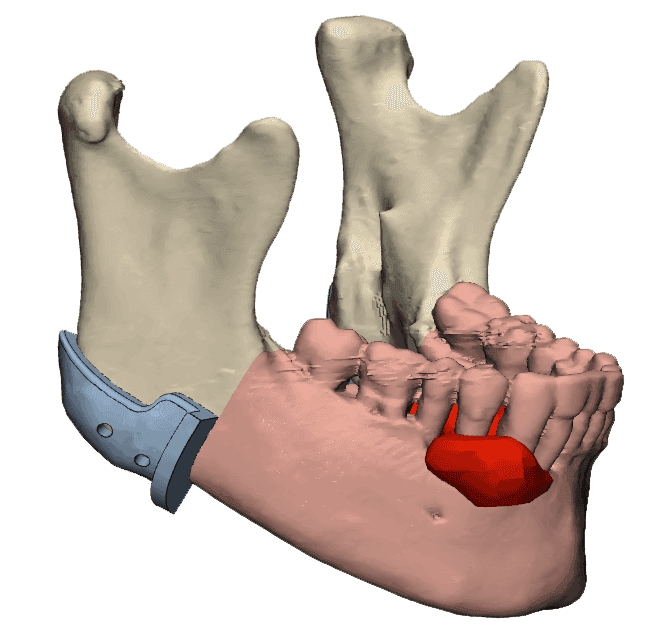
Patienter diagnosticeret med hoved-hals-kræft med indvækst i underkæben bliver vurderet på en multidisciplinær teamkonference, hvor operationsindikation og -metode besluttes af øre-næse-hals-kirurger, plastikkirurger, kæbekirurger og onkologer. Ud fra en præoperativ CT af hoved-hals-området 3D-printer kliniske ingeniører en model af patientens underkæbe med tydelig markering af tumoren (Figur 1A), hvilket er et anvendeligt redskab til kommunikation med patienten og for teamets operationsplanlægning. Ved beslutning om rekonstruktion af underkæben med en fri fibulaknoglelap får patienten foretaget en CT-angiografi af begge underben, og denne anvendes til at vurdere fibulas blodforsyning og til senere virtuel operationsplanlægning.
Virtuel operationsplanlægning
Efter den præoperative konsultation mødes kirurger og ingeniører til virtuel planlægning af den eksakte resektion af underkæbeknoglen med sikkerhedsafstand fra tumor (typisk min. 1 cm), som markeres på den præoperative CT (Figur 1B). Ud fra placering og størrelse af tumor i forhold til underkæbens kurve kan der være behov for ét lige stykke fibulaknogle eller flere mindre fibulasegmenter, der samles i vinkler (Figur 1C + D + E). På CT-angiografien af underbenet positioneres fibulasegmenterne, så den bedst egnede knoglelap høstes med hensyn til længden af segmenterne med planlagte vinkler og sikker blodforsyning. Ved behov for bløddelsrekonstruktion af mundhulen kan CT-angiografi af underbenet benyttes til visualisering af blodforsyningen til et hudområde over fibula, så et passende hudområde kan medtages, når fibulaknoglelappen høstes [5].
Fremstilling af 3D-printede patientspecifikke modeller
Når operationsdesignet er planlagt, 3D-printes en model af den nye underkæbe (inklusive fibulasegmenter) i plastmateriale (bionedbrydelig polymer), så titaniumskinnen til fiksering af den rekonstruerede underkæbe kan formes ud fra modellen og herefter steriliseres inden operationen. Derudover 3D-printes patientspecifikke skæreguider til brug under operationen. Disse guides klikkes på knoglen og bestemmer placering og vinkling af osteotomierne både ved partiel resektion af underkæben og ved udskæring af knoglesegmenter fra fibula. Skæreguider fremstilles ligeledes i et plastmateriale (fotopolymer), som kan autoklaveres inden operationen.
Operationen
Øre-næse-hals-kirurger og kæbekirurger samarbejder om resektion af det patologiske segment af underkæben ved anvendelse af de 3D-printede skæreguider, som fikseres på underkæben (Figur 1B). Synkront med fjernelse af det patologiske område høster plastikkirurgerne den frie fibulaknoglelap fra underbenet. Dette foregår ligeledes ved hjælp af 3D-printede skæreguider, som fikseres på fibula for at sikre korrekt orientering og vinkel af knoglesegmenterne (Figur 1C). Knoglelappens blodforsyning forbliver intakt, indtil resektionen af det patologiske område er afsluttet, og radikalitet er bekræftet ved frysemikroskopi. Ved behov for halsdissektion udføres denne, og relevante blodkar frilægges og bevares. Herefter overskæres knoglelappens blodforsyning, og fibulaknoglesegmenterne placeres og fikseres til underkæben ved hjælp af de præformede titaniumplader, så fibulasegmenterne passer i underkæbedefekten (Figur 1D + E). Efter korrekt placering og fiksering af knoglesegmenterne genetablerer plastikkirurgerne knoglelappens blodforsyning ved mikrokirurgiske anastomoser til blodkar i hoved-hals-området. Fra underbenet er der ved knoglelappen ofte medtaget et hudområde, som benyttes til rekonstruktion af intraorale bløddele, og efter indsyning af denne afsluttes operationen.
Konventionel frihåndskirurgi ved rekonstruktion af underkæben med fri fibulalap leverer gode resultater, men metoden kræver stor erfaring og præcision, da den er baseret på øjemål [6]. 3D-assisteret kirurgi med præoperativ virtuel planlægning og 3D-printede skæreguider er blevet et populært værktøj, som kan være med til at optimere og forbedre den rekonstruktive proces [4].
Fordele ved 3D-print
3D-assisteret kirurgi har en række veldokumenterede fordele sammenlignet med konventionel kirurgi. Metoden kan være med til at nedsætte både den samlede operationstid og iskæmitiden for knoglelappen (tiden fra overskæring af knoglelappens blodforsyning på underbenet til genetablering af blodforsyningen ved ansigtet) [4, 7]. Metaanalyser har dog ikke dokumenteret forskelle i lapnekrose og komplikationsrater, når man sammenligner 3D-assisteret rekonstruktion af underkæben med frihåndskirurgi [4, 7]. Som yderligere fordel tyder flere studier på kortere indlæggelsestid ved 3D-assisteret rekonstruktion af underkæben [4, 8].
3D-assisteret kirurgi med præoperativ virtuel planlægning giver en unik mulighed for skræddersyede, patientspecifikke resultater [9], som kan forbedre både de funktionelle og æstetiske resultater [2, 7]. Den virtuelle planlægning tager højde for knoglesnit i alle tre planer, hvilket kan være udfordrende på øjemål [5, 10]. Der kan fremstilles patientspecifikke titaniumsskinner til fiksering af underkæben, og disse øger styrken ved fiksering. Præcise rekonstruktioner giver øget knogle til knogle-kontakt [3] og kan reducere smerter samt sikre bedre okklusion og æstetik [7, 11]. 3D-assisteret kirurgi giver ligeledes mulighed for operation af komplekse cases med brug af flere fibulasegmenter [2, 4, 7] uden at øge komplikationsraten [4, 7, 12]. Den virtuelle planlægning kan desuden visualisere blodforsyningen til hudområdet over fibula, så kirurgen kan udvælge hudområdet hensigtsmæssigt i forhold til udskæring af knoglelappen [10].
Endelig kan 3D-printede modeller af henholdsvis underkæben med tumor og den rekonstruerede underkæbe med fibulasegmenter øge patientforståelsen for det planlagte indgreb. Desuden er de 3D-printede modeller et gavnligt værktøj, når kirurgerne skal markere og planlægge tumorresektionen. Dette er med til at sikre konsensus mellem de samarbejdende kirurgiske specialer og øger forudsigeligheden af operationen.
Ulemper ved 3D-print
De primære ulemper ved 3D-assisteret kirurgi er de økonomiske omkostninger [5, 7] samt den ekstra præoperative planlægningstid i forbindelse med virtuelle eller fysiske planlægningsmøder med ingeniørerne [5]. Ved brug af kommercielle udbydere afsætter kirurgerne tid til at overføre skanningsbilleder, gennemføre virtuel operationsplanlægning via telekonference og endelig godkendelse af 3D-modeller. Derudover går der tid med at fremstille og levere modellen, før operationen bliver udført. Den potentielt lange leveringstid ved brug af kommercielle udbydere (op til tre uger [13]) er en nævneværdig ulempe, da forlænget ventetid fra diagnostik til operation har betydning for overlevelsen af patienter med hoved-hals-kræft [14]. De nationale retningslinjer for behandling af hoved-hals-kræft i Danmark anbefaler maks. syv dages ventetid fra endelig diagnostik og beslutning om kirurgisk behandling til selve operationen [15]. Dertil kommer også lovkrav om, at operation af hoved-hals-kræft skal ske inden for 14 kalenderdage, fra patienten har givet samtykke til operationen. Dette kan ikke altid imødekommes, når man skal vente på de kommercielle udbydere [13].
Manglende erfaring med frihåndskirurgi er en udfordring, hvis der er behov for intraoperativ ændring af resektionsafstanden [5, 8, 16]. F.eks. hvis en tumor er progredieret siden skanning eller ved uforudset udbredelse af kræftsygdommen, hvor man ikke opnår radikalitet ved den frysevejledte mikroskopi ud fra de planlagte snit. Det kan derfor være nødvendigt på forhånd at designe en ekstra (bredere) resektionsafstand [5].
Priser for virtuel planlægning og 3D-print hos kommercielle leverandører varierer fra 15.000 til 30.000 kr. pr. patient [13]. Dog opvejer reduktionen i operations- og iskæmitid, den øgede kvalitet af rekonstruktionen samt de potentielt færre komplikationer og eventuelt kortere indlæggelsestid [8] muligvis de øgede omkostninger. Der er ikke gennemført randomiserede kliniske studier, som sammenligner langtidseffekterne efter henholdsvis 3D-assisteret kirurgi og konventionel frihåndskirurgi [4].
In-house 3D-print
Det stigende behov for 3D-assisteret kirurgi har fået flere hospitaler til at etablere in-house 3D-centre. Etablering af et in-house 3D-center forudsætter en indledende etablerings- og læringsfase. Derefter vil både produktionstid og omkostninger nedsættes væsentligt [13, 17]. Dette gør 3D-assisteret kirurgi tilgængelig for flere patienter, uden at patientrettigheder for ventetid overskrides. Ved at ansætte kliniske ingeniører på hospitalet lettes logistikken for den præoperative virtuelle planlægning markant. En fordel er, at produktionen af skæreguider kan igangsættes, umiddelbart efter at operationsindikationen er stillet. En anden fordel er, at ingeniørerne kan observere de 3D-assisterede operationer, hvilket øger læring og innovation mellem kirurger og ingeniører [18]. Hvis kirurgerne selv skal stå for den virtuelle planlægning og 3D-print, vil det medføre betydelig ekstra arbejdstid for klinikerne, som heller ikke umiddelbart besidder de rette teknologiske kompetencer [13]. Med et in-house 3D-center kan de patientspecifikke skæreguider være printet, autoklaveret og klar til operationen, allerede tre dage efter operationsindikationen er stillet [13]. Desuden kan etablering af et in-house 3D-center fordre bredere brug af 3D-modeller i andre kirurgiske specialer. Hospitalets behov for 3D-assisteret kirurgi skal dog være stort, før et in-house 3D-center er økonomisk rentabelt.
3D-assisteret kirurgi har udviklet den rekonstruktive kirurgi og er blevet en tilgængelig behandling for flere patienter [19]. Aktuelt anvendes 3D-assisteret kirurgi primært ved knoglekirurgi, men i takt med den fortsatte udvikling vil også bløddelskirurgi kunne planlægges med virtuelle og fysiske 3D-modeller. Mere futuristisk forventes en rivende udvikling i 3D-bioprint, så biologisk materiale kan fremstilles til direkte rekonstruktion [19].
Korrespondance Lasse Østrup Petersen. E-mail: lasse.oe.petersen@gmail.com
Antaget 6. august 2024
Publiceret på ugeskriftet.dk 2. september 2024
Interessekonflikter ingen. Forfatternes ICMJE-formularer er tilgængelige sammen med artiklen på ugeskriftet.dk
Referencer findes i artiklen publiceret på ugeskriftet.dk
Artikelreference Ugeskr Læger 2024;186:V04240267
doi 10.61409/V04240267
Open Access under Creative Commons License CC BY-NC-ND 4.0
Preoperative virtual surgical planning and the use of 3D-printed patient-specific models and cutting guides are increasingly being used in the reconstruction of mandibular defects with a free bone flap. This technology offers several advantages over conventional surgery, such as reduced operating time, reduced bone flap ischaemia time, and the ability to perform more complex and precise reconstructions. This review presents the evidence supporting 3D-assisted surgery for mandibular defect reconstruction and discusses the utilisation of commercial vendors versus in-house 3D-printing solutions.