Endoskopisk fjernelse af lumbal discusprolaps

Jacob Holmen Terkelsen, Mikkel Rune Otte Kunwald, Torben Hundsholt & Carsten Reidies Bjarkam
Hovedbudskaber
Den tekniske udvikling har reintroduceret endoskopiske teknikker til behandling af degenerativ lænderygsygdom.
Adgang til spinalkanalen sker interlaminært eller transforaminalt.
I forhold til åben kirurgi synes særligt den transforaminale adgang fordelagtig til fjernelse af visse former for paramedian og/eller foraminal prolaps.
Den første intenderede fjernelse af en lumbal discusprolaps blev beskrevet i 1934 [1]. Året efter foretog man på Rigshospitalets nyoprettede neurokirurgiske afsnit den første danske operation [2]. Det var på dette tidspunkt diagnostisk og kirurgisk en omfattende procedure, da den kliniske diagnose måtte verificeres ved intratekal indgift af oliejodkontrast og efterfølgende røntgenundersøgelse, mens selve prolapsfjernelsen foregik ved en større åbning af hvirvelbuens bagre del (laminektomi over 1-3 niveauer), hvorefter man tilgik prolapsen transduralt [2]. Betydelige sårsmerter, likvorfistler og araknoiditis var således hyppige komplikationer, hvilket også afspejlede sig i, at den første danske patient postoperativt var immobiliseret i 17 dage og først blev udskrevet efter 54 indlæggelsesdage [2]. Den transdurale adgang blev hurtigt afløst af en lateral paradural adgang, hvorved man kunne bevare duras integritet og undgå intenderede likvorfistler, ligesom den kirurgiske åbning af hvirvelbuen med stigende erfaring kunne minimeres til en partiel hemilaminektomi for de fleste prolapsers vedkommende [2]. Diagnostikken er blevet betydeligt mere skånsom og præcis med fremkomsten af CT- og MR-skannere [3], hvilket ligeledes har haft betydning for planlægning af den mest skånsomme/minimale kirurgiske adgang til prolapsen [4]. Endelig har tilkomst og brug af operationsmikroskop til optimal belysning og forstørrelse af det kirurgiske felt yderligere forbedret indgrebets udførelse og sikkerhed [5, 6]. En kyndig fjernelse af en førstegangs lumbal discusprolaps (mikrokirurgisk diskektomi) er således i dag et mindre kirurgisk indgreb (30-90 min, 50-200 ml blødning, cikatricelængde 3-5 cm) [7].
I håb om at minimere det kirurgiske adgangstraume yderligere forsøgte man allerede for mere end 30 år siden at tilgå prolapsvævet endoskopisk [8, 9]. Introduktionen var dog, også på vores center, mindre succesfuld af flere årsager, hvoraf de vigtigste var, at endoskopiudstyret ikke var designet specielt til lænderygkirurgi og ofte teknisk dårligt, ligesom besværet og begrænsningerne ved proceduren slet ikke stod mål med den forventede gevinst i form af et mindre kirurgisk traume [9]. Sagt med andre ord, det tog alt for lang tid, der var for mange tekniske komplikationer, og for mange indgreb måtte alligevel konverteres til åben kirurgi.
Til trods herfor forsatte særligt tyske og asiatiske centre, med at foretage endoskopisk prolapsfjernelse og vandt efterhånden god erfaring hermed [10, 11], ligesom den forsatte brug og tekniske udvikling har medført, at der nu foreligger specielt adgangsudstyr og -teknikker, endoskoper, instrumenter og monitorer til endoskopisk lænderygkirurgi [9].
Endoskopisk lænderygkirurgi er således igen blevet tiltagende populært [9] og blev på denne baggrund også reintroduceret på vores center i efteråret 2020.
Den perkutane indførsel af endoskop til spinalkanalen kan ske via to adgangsveje (Figur 1) [11, 12].
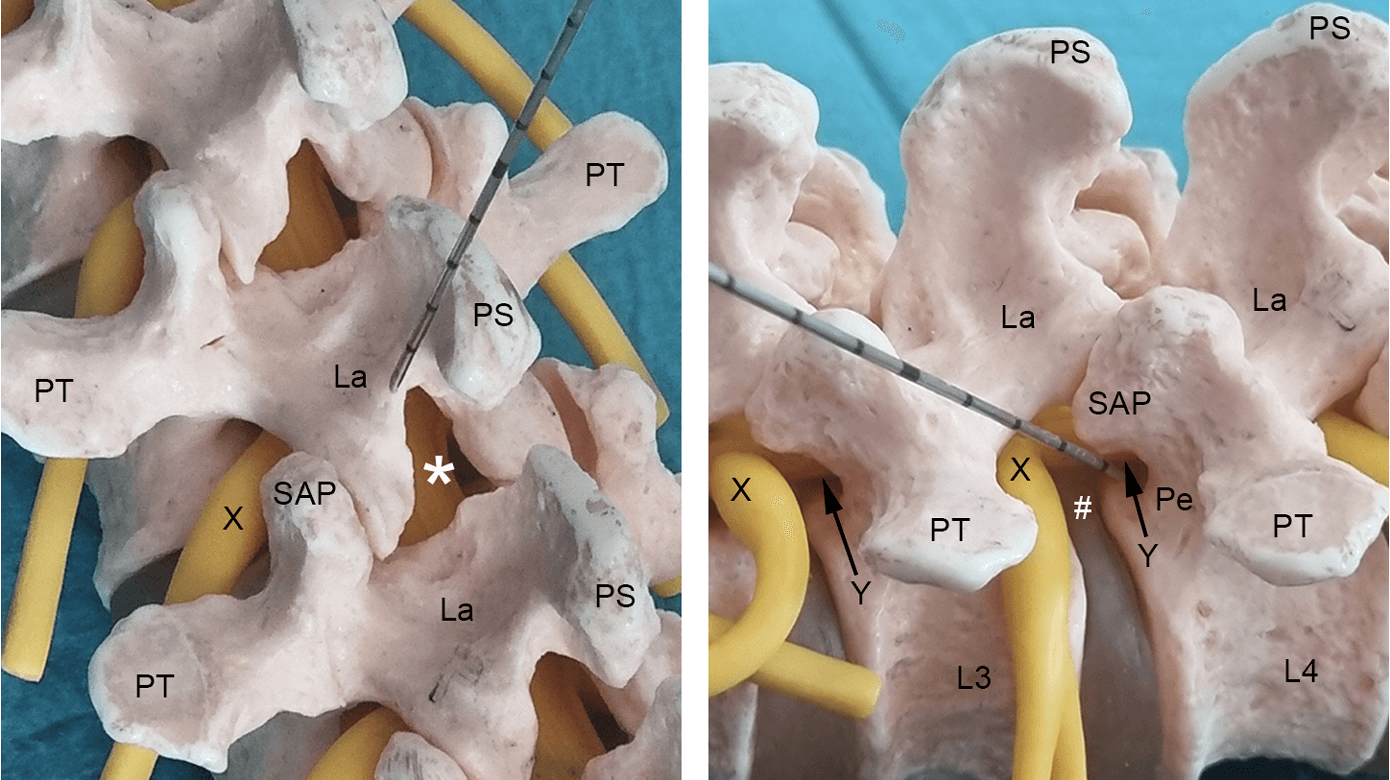
Den interlaminære adgangsvej (Figur 1 A) ligner den klassiske mikrokirurgiske åbning, hvor man via en mindre (maks. 1-2 cm) paramedian rygincision indfører dilatatorer og guiderør, så endoskopet ender på underkanten af lamina (Figur 1 A) ved overgangen til det interlaminære rum dækket af ligamentum flavum. Man kan nu under skopvisualisering og med de rette instrumenter fjerne ossøs lamina og tilstødende flavum, hvorved man ultimativt vil frilægge durasækkens dorsalside. Med denne som udgangspunkt kan man hernæst følge durasækken lateralt og ventralt, hvorved man vil nå spinalkanalens reces med afgående nerverod og protruderende discusvæv. Den interlaminære teknik er velegnet til lænderygsøjlens nederste niveauer (L3/L4, L4/L5, L5/S1), hvor det interlaminære rum er særligt stort, og kan her bruges til behandling af central og lateral spinalstenose (grundet ligamentum flavum-hypertrofi), og/eller paramedian prolapsfjernelse [9-12].
Den transforaminale adgangsvej (Figur 1 B) fordrer, at man får indført sit endoskop igennem foramen intervertebrale uden at lædere den foraminalt udtrædende rod [12]. Man bruger derfor et smallere endoskop, ligesom man ofte udnytter, at man ossøst kan udvide foramen dorsolateralt ved delvist at afrimme facetledets nedefrakommende superiore artikulerende proces (Figur 1 B) [12]. Endoskopets endemål er at stå ud for den nederste del af discus, hvor pediklen har sin indre og kranielle afgrænsning, så man møder den afgående rod i recessen (Figur 1 B), hvor en paramedian prolaps ofte kan udøve rodtryk. Ønskes en foraminal frilægning af den ovenfrakommende udgående rod sigtes knap så medialt, så endoskopet ender mere lateralt ud for discus i foramen (Figur 1B).
En perkutan transforaminal endoskopisk diskektomi (PTED) starter med, at man røntgenvejledt planlægger sine sigtelinjer til målområdet i anteriort-posteriort plan (Figur 2 A) og sideplan (Figur 2 B) og på huden markerer, hvor sigtelinjerne mødes 8-12 cm fra lænderyggens midte (Figur 2 C). Her anlægges lokalanæstesi, hvorefter man herfra under røntgenvejledning og under manuel monitorering af aktivitet i n. ischiadicus indfører sin søgekanyle gennem foramen mod målområdet (Figur 2 C). K-tråd placeres, og over denne indføres hernæst en række dilatatorer og rimmere (Figur 2 C indsat lille billede), så man via den superiore artikulerende proces (Figur 1) ossøst får skabt så megen plads, at endoskopets arbejdsrør kan indføres (Figur 2 D). Man kan nu direkte visualisere målområdet (Figur 3 A) med discusspalten med protruderet discusvæv kl. 6, pediklen kl. 9, den afrimmede superiore artikulerende proces kl. 12 og foramen med udgående rod kl. 3 (Figur 3 B). Discusvæv fjernes herefter, hvorved man, som frilægningen skrider frem, først vil møde epiduralt bindevæv og flavum og slutteligt få indblik til nerveroden, som derved er frilagt (Figur 3 C). Endoskopet og indføringsrøret kan hernæst fjernes, og hudåbningen lukkes med en enkelt sutur (Figur 3 D). Efter en time på opvågningen overgår patienterne til stamafdelingen, hvor de mobiliseres mhp. udskrivning 2-3 t. senere samme dag. Med forbehold for vanligt brug af smertestillende medicin, kan de fleste patienter postoperativt nøjes med paracetamol 1 g × 4, og NSAID 400 mg p.n. maks. × 3 pr. døgn. Suturen (Figur 3 D) fjernes ved egen læge efter 8-10 dage.
Patoanatomiske forudsætninger for perkutan transforaminal endoskopisk diskektomi
Da PTED fordrer transforaminal adgang, er det vigtigt, at foramen (Figur 1 B) har en passende højde [11, 12], hvilket ofte er proportionalt med discushøjden, som desværre aftager med alderen. Ligeledes kan man særligt hos mænd, hvor hoftebenskammen er høj, få problemer med at få adgang til L5/S1-foramen [11, 12].
Da endoskopets arbejdsfelt og manøvremuligheder i forhold til åben kirurgi trods alt er begrænset [11, 12], bør frilægningens omfang være tilpassende afgrænset. Omfattende og udbredte rodfrilægninger klares bedst med åben kirurgi (man får det hele med). Ligeledes kræver hvert niveau og side separat indstik med endoskopet, hvorfor endoskopkirurgi tidsmæssigt i forhold til åben kirurgi er bedst egnet til ensidig prolapsdannelse på et niveau.
Tilstande, hvor perkutan transforaminal endoskopisk diskektomi er særlig fordelagtigt i forhold til åben mikrokirurgisk frilægning
Er ovenstående patoanatomiske forudsætninger til stede, bør man i forhold til åben mikrokirurgisk dekompression bemærke, at: 1) PTED er velegnet til mange former for foraminal prolaps [11], da åben frilægning af disse ofte nødvendiggør fjernelse af facetleddet og derfor indebærer en risiko for instabilitet, som i værste fald kan nødvendiggøre stivgørende kirurgi, hvorved vævstraume og operationstid øges betydeligt, ligesom stivgøringen på sigt giver risiko for slidgigtsudvikling (adjacent disc disease) på naboniveauerne [13]. 2) PTED er lige godt til tynde som kraftige patienter, da målsøgning og arbejdsvilkår er de samme, lige meget hvor dybt endoskopet indføres, hvorimod åben kirurgi besværliggøres, jo mere overvægtig patienten er, ligesom efterfølgende sårheling ofte er problematisk [14]. 3) PTED er godt til recidivprolapser, da man pga. den alternative (transforaminale) vej til prolapsen undgår arvæv dannet efter tidligere åben kirurgi [11].
Læringskurven kan være problematisk ved perkutan transforaminal endoskopisk diskektomi
Traditionelt uddannede rygkirurger er ikke fortrolige med endoskopkirurgi [15]. Ligeledes indebærer PTED-teknikken en ny måde at tilgå og se spinalkanalens anatomiske strukturer på, hvorfor de fleste må påregne en længere optræningsperiode, før de føler sig helt fortrolige med indgrebet (læringskurven er lang og træg) [15-17]. Det er af samme årsag velkendt, at der særligt i starten ofte vil være nogle patienter, som skulle have fået foretaget PTED, som må konverteres til åben kirurgi, fordi man under operationen ikke kan tilgå prolapsen [15-17]. På samme måde vil der initialt være patienter, som grundet endoskopets begrænsede manøvre- og udsynsmuligheder ikke får fjernet nok prolapsvæv, så ny frilægning bliver nødvendig [15-17]. Det er derfor særlig vigtigt, at man betænker og i sin patientinformation omtaler disse forhold.
Aktuel evidens for perkutan transforaminal endoskopisk diskektomi i forhold til åben mikrokirurgisk frilægning
Der foreligger nu flere metaanalyser [18-21] og større sammenlignende studier [22, 23] samt enkelte velgennemførte randomiserede undersøgelser [24, 25], som viser, at til de rette patienter (se ovenstående) er PTED minimalt invasiv, hurtig og noninferior til den traditionelle mikrokirurgiske adgang [18-24], da de to teknikker har ligeværdige resultater ved intermediær opfølgning og langtidsopfølgning, når man kigger på hårde effektmål som reduktion af bensmerter og funktionsniveau [20].
Særligt bemærkelsesværdigt er et randomiseret hollandsk studie, hvor man efter en indkøringsfase kunne overgå til at operere patienterne i lokalbedøvelse og med en gennemsnitlig operationstid på 30 min [24]. Der er ligeledes fundet, at PTED sundhedsøkonomisk på disse vilkår til trods for dyrere udstyrsomkostninger til selve operationen grundet kortere indlæggelsestid og hurtigere restitution er mere fordelagtigt end den vanlige mikrokirurgiske adgang [25].
Endoskopisk lænderygkirurgi har udviklet sig til et brugbart addendum til de eksisterende rygkirurgiske teknikker, da særligt den perkutane transforaminale adgang i visse situationer tillader smart og minimalt invasiv dekompression af paramediane og foraminale prolapser samt recidivprolapser. For korrekt selekterede patienter kan PTED således på sigt bidrage til at støtte transitionen fra kirurgisk behandling af lumbal discusprolaps i fuld bedøvelse under indlæggelse til sammedagskirurgi udført i lokalanæstesi.
Korrespondance Carsten Reidies Bjarkam. E-mail: c.bjarkam@rn.dk
Antaget 19. september 2023
Publiceret på ugeskriftet.dk 23. oktober 2023
Interessekonflikter ingen. Forfatternes ICMJE-formularer er tilgængelige sammen med artiklen på ugeskriftet.dk
Referencer findes i artiklen publiceret på ugeskriftet.dk
Artikelreference Ugeskr Læger 2023;185:V05230322
Jacob Holmen Terkelsen, Mikkel Rune Otte Kunwald, Torben Hundsholt & Carsten Reidies Bjarkam
Ugeskr Læger 2023;185:V05230322
The technical development has caused a reintroduction of endoscopic techniques directed towards degenerative spine disease. A summary of the endoscopic procedure is given in this review. The spinal canal is reached through an inter-laminar or transforaminal access. In comparison with open surgery the percutaneous transforaminal access seems especially advantageous for the removal of paramedian and/or foraminal herniated disc material. However, careful patient selection is required, as the restricted manoeuverability and working zone of the endoscope and patient specific pathoanatomy in some cases will disfavour endoscopy.