Førsteprincipræsonnement i klinisk diagnostisk tænkning

Muhammad Sabbah1, 2, 3
Hovedbudskaber
Rollen som medicinsk ekspert er utvivlsomt den vigtigste lægerolle. Et nøgletræk ved medicinsk ekspertise er evnen til at kategorisere patientens problem – at stille den korrekte diagnose. Ikke desto mindre er den diagnostiske fejlrate estimeret til at være 10-15% [1, 2], og den er stort set uændret gennem det seneste århundrede [3]. Derfor er der et uforløst potentiale i forbedringen af patientbehandling gennem optimering af lægers diagnostiske træfsikkerhed. Formålet med denne artikel er at adressere følgende spørgsmål i lyset af den seneste psykologiske forskning inden for diagnostisk tænkning:
Klinikeren har sjældent – hvis nogensinde – fuldkommen adgang til samtlige relevante oplysninger, hvorfor den diagnostiske proces i sin natur er probabilistisk, involverende en vis irreducibel usikkerhed. Samtidig skal lægen navigere gennem utallige situationelle, patient- og klinikerrelaterede variable, som kan komplicere den diagnostiske proces i alle dens faser [4] (et uddrag er vist i Figur 1). Sygdomme er dynamiske størrelser, der kan progrediere nonlineært, og de kan have talrige symptomer, som kan udvise interindividuel variation. Eksempelvis vil ikke alle symptomer på en sygdom nødvendigvis manifestere sig i alle patienter, og ikke alle patienter afficeres nødvendigvis af ethvert givent symptom – hverken objektivt eller subjektivt. Sygdomme kan præsentere sig atypisk, og debut og progression kan udvise temporal variation – fra sekunder (f.eks. vaskulære lidelser) til år (f.eks. degenerative lidelser). Det stadie i sygdommen, som patienten undersøges i, kan derfor afgøre, om lægen spores ind på den korrekte diagnose tidligt i udredningen.
I takt med stigende levealder bliver komorbiditeter mere hyppigt forekommende. En sygdom kan modificere symptomerne på en anden (f.eks. diabetisk autonom neuropati på debuten af akut myokardieinfarkt), og kroniske sygdomme kan modulere patientens baseline-fysiologi (f.eks. kronisk forhøjet CO2-tension hos patienten med KOL) og dermed påvirke præsentationen af en ny sygdom. Med talrige komorbiditeter følger typisk også livslang polyfarmaci, som kan modificere symptomers sværhedsgrad, progression og temporale udvikling.
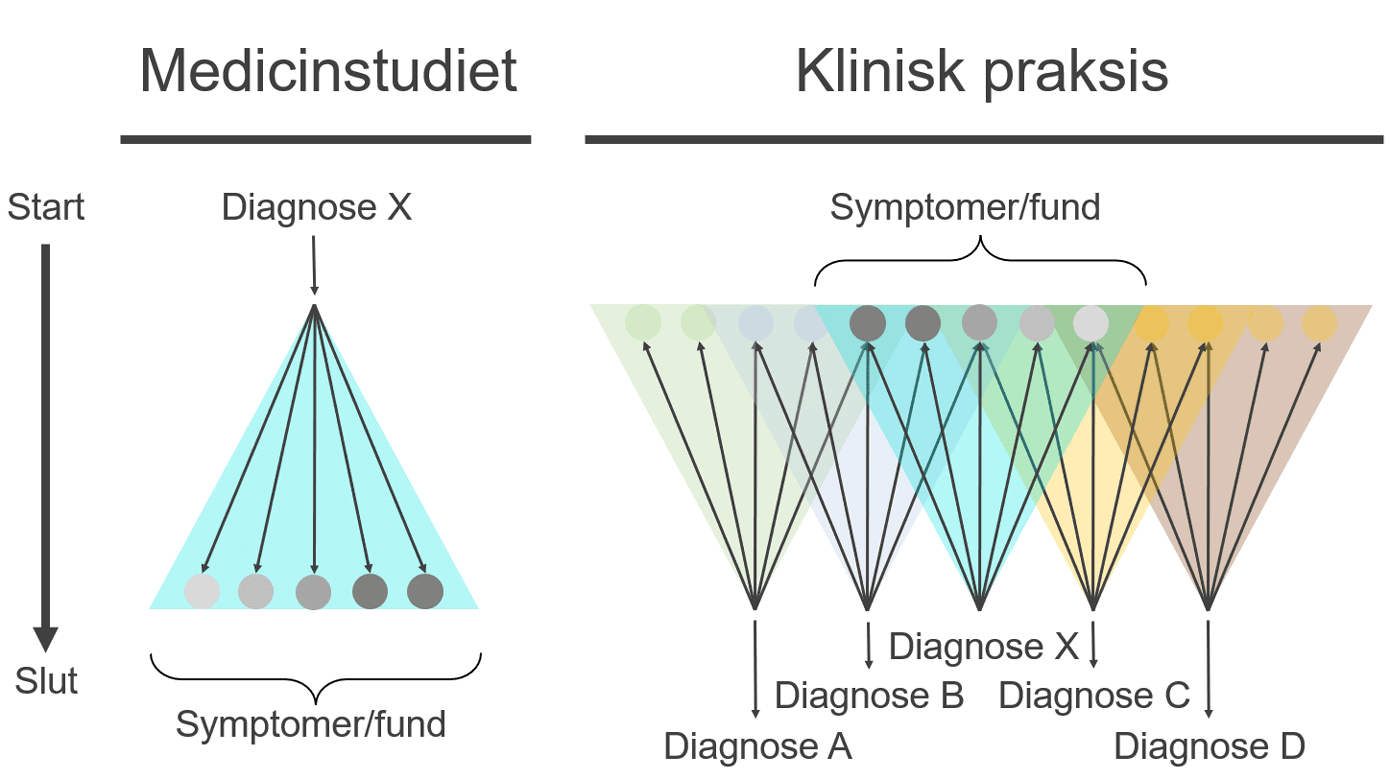
Det er anslået, at mindst 50 forskellige faktorer kan komplicere den diagnostiske proces [4]. Af disse er kognitive bias en af de vigtigste årsager til fejldiagnosticering [1]. Mindst 50 forskellige bias er vurderet at have relevans for diagnostisk tænkning [1, 5, 6] (et uddrag er vist i Tabel 1 baseret på [6, 7]). Ydermere består undervisningsmaterialet på medicinstudiet overvejende af lærebøger med lineære gennemgange af sygdommes ætiologi, patogenese, patofysiologi, symptomer osv. I skarp kontrast til dette præsenteres den yngre læge typisk for patienter med konstellationer af symptomer, som passer med flere kliniske sygdomsenheder (Figur 2). Dog har der i de senere år været øget fokus på symptomorienteret diagnostik bl.a. gennem problembaseret læring [8].
Klinisk diagnostisk tænkning (diagnostic reasoning) er en kompleks, multifacetteret og idiosynkratisk færdighed, som, jævnfør de sidste 50 års forskning, har vist sig vanskelig at studere [9]. Studiet af tankeprocesser falder ind under den kognitive psykologi, hvor den fremherskende deskriptive model af generel tænkning – den såkaldte Dual Process Theory – integrerer to fundamentalt forskellige tilgange til tænkning: den intuitive og den analytiske [10]. Disse kaldes også hhv. System 1- og System 2-tankeprocesser.
System 1 er automatisk, associativ/kontekstspecifik, hurtig, reflektorisk/ubevidst, effektiv og præget af intuition og mønstergenkendelse indlært gennem praktisk erfaring. Ulempen er sårbarhed for fejl pga. bias, fraværet af videnskabelig stringens og krav om intern logisk konsistens. System 2, derimod, er bevidst, analytisk, systematisk, logisk konsistent og videnskabeligt stringent, men også tidskrævende, ineffektiv og mentalt udfordrende.
Et klinisk eksempel på System 1-tænkning er, når lægen f.eks. ser et unilateralt, vesikulært udslæt, skarpt afgrænset til ét dermatom, og straks – nærmest automatisk – genkender det som herpes zoster. Omvendt vil patienten med det diffuse symptombillede på tværs af mange organsystemer tvinge lægen til at yde en bevidst, kognitiv indsats i analysen og integrationen af oplysninger fra anamnese, objektiv undersøgelse og parakliniske prøvesvar for at finde diagnosen, dvs. en System 2-tilgang.
I praksis er der dog et komplementært og dynamisk samspil mellem System 1- og System 2-tænkning i den diagnostiske proces [11]. Lægens initiale indtryk kan f.eks. foranledige en hurtig formulering af få differentialdiagnoser (System 1), som efterfølgende underkastes systematisk analyse (System 2). Dual process-modellen er ikke blot teori, idet nyere studier underbygger modellen eksperimentelt [12-14]. Især inden for almen- og akutmedicin – specialer med en bred, uselekteret og udifferentieret patientpopulation – har teorien en plads som en deskriptiv model [15].
Generelt gælder det, at den nyuddannede læge initialt læner sig op ad sin biomedicinske viden fra studiet, når vedkommende skal stille diagnoser (System 2) [4]. Efter repetitiv eksponering for sammenlignelige cases opbygger den pågældende gradvist en mental abstraktion – et såkaldt sygdoms-script (illness script) – som kortlægger den »prototypiske patient« i forhold til symptomer og deres kronologi, men også evt. prækonditionerende helbredsmæssige, livsstilsmæssige og sociale faktorer for sygdommen [16]. Dette script fremkaldes hurtigt og automatisk, næste gang en patients klager matcher scriptet. Jo flere patienter lægen eksponeres for, desto mere raffineret bliver sygdoms-scriptet. Således vil den erfarne kliniker også lagre scripts for specifikke patientforløb, f.eks. pga. en særlig, atypisk præsentation eller andet, som afviger fra den prototypiske patient. Med andre ord vil novicen i reglen bevæge sig fra System 2- mod System 1-dominant tænkning i takt med, at den kliniske erfaring øges [4]. Her det vigtigt at understrege, at klinisk erfaring ikke nødvendigvis er synonymt med ekspertise [17-20]. Forskellige strategier er foreslået for at gardere klinikeren mod System 1-fejl, herunder fremmelse af kritisk tænkning, metakognition og opmærksomhed på kognitive bias [4, 9, 21-23].
I et fåtal af cases undslipper diagnosen System 1 og indledende System 2-forsøg hos selv de mest erfarne klinikere. Med andre ord er der behov for en dedikeret System 2-tilgang. For at være objektiv og grundig må lægen suspendere det mentale netværk af heuristikker, der normalt faciliterer vedkommendes effektive kliniske virke, til fordel for en langsommere, men også mere analytisk, finkornet og biologisk stringent tilgang. Hvordan man som kliniker konkret praktiserer System 2-tænkning er mindre klart beskrevet i litteraturen.
Oftest møder man beskrivelsen »hypothetico-deductive« [11], men der er også nyere forsøg på at kortlægge processen yderligere [24]. Undertegnede foreslår her en præskriptiv model, der tager udgangspunkt i en tilpasning af førsteprincipræsonnement (first principles reasoning, FPR) til en klinisk kontekst. FPR er en kognitiv analysemetode, der kan spores tilbage til Aristoteles. Førsteprincipper er fundamentale, selvforklarende propositioner, der ikke kan deduceres fra mere fundamentale propositioner. FPR er en måde at tilgå et problem, hvor man suspenderer sin forudindtagede opfattelse af problemets struktur og i stedet analyserer problemets fundamentale elementer – dets førsteprincipper.
Ud fra disse ræsonnerer man sig op igennem problemet. Man dekonstruerer altså informationen i casen og analyserer de enkelte elementer, før man rekonstruerer informationen til et sammenhængende billede foreneligt med en eller få biologisk plausible diagnoser.
Hvad udgør så førsteprincipperne i klinisk medicin? Hvilken opløsning af detaljer kan betragtes som fundamental? Hvor langt tilbage, rent biomekanistisk, skal man spore symptomer og abnorme fund? Det pragmatiske svar er: så langt tilbage som påkrævet for at levere en biologisk sammenhængende forklaring på casens indiskutable sandheder. I visse tilfælde vil en makroskopisk analyse af anatomiske og fysiologiske fund være tilstrækkelig (f.eks. indre blødning), mens man i andre tilfælde ender på DNA-niveau (genetiske syndromer). Figur 3 illustrerer en skabelon for System 2-tænkning i komplicerede kliniske cases.
Et eksempel på en FPR-analyse: patienten med dyspnø som primær klage. I stedet for at gennemgå listen af sygdomme, der forårsager dyspnø, stiller man spørgsmålet: Hvilke underliggende patofysiologiske mekanismer kan forårsage dyspnø? Givet at dyspnø skyldes hypoxæmi, må problemet involvere ilttilbud, -absorption eller -forbrug. Alternativt korrigerer dyspnøen en anden forstyrrelse eller har en nonorganisk/psykiatrisk årsag. Konkrete årsager er hhv. mekanisk obstruktion i de konduktive luftveje, øget diffusionsafstand, nedsat gasudvekslingsareal, abnorm iltbindingskapacitet, nedsat kapacitet til ilttransport eller metabolisk acidose. Bemærk, at man endnu ikke kommer ind på diagnoser, da man i denne fase eksplorerer de plausible patofysiologiske mekanismer (Figur 3). Hver af disse mekanismer kan være et led i mange forskellige sygdomme, f.eks. kan mekanisk obstruktion skyldes et fremmedlegeme, mucusprop, tumorindvækst m.fl. Øget diffusionsafstand kan bl.a. skyldes fibrose, lungestase. Imidlertid må og skal alle sygdomme, der forårsager dyspnø, konvergere mod de grundlæggende årsager nævnt ovenfor. Således kan de betragtes som førsteprincipper i analysen af dyspnø og danne grundlaget for en søgning efter konkrete patofysiologiske mekanismer. Den øvelse vil hurtigt dilatere det »kausale spektrum« betragteligt. Det konstrikteres imidlertid igen, når alle casens negative anamnestiske, objektive og parakliniske fund inddrages i analysen. Tilbage er et mindre antal biologisk velbegrundede differentialdiagnoser, der har undergået stringent System 2-analyse (Figur 3).
Diagnostisk tænkning er en af lægens vigtigste kernekompetencer. I en travl hverdag vil klinikeren hovedsageligt læne sig op ad hurtig og effektiv System 1-tænkning. Imidlertid fordrer særligt komplicerede cases en mere analytisk tilgang, som typisk involverer indgående biomedicinsk viden. Paradoksalt nok vil den viden typisk være fjernere for den seniore kliniker sammenlignet med den yngre læge. Omvendt besidder den unge læge ikke det velkalibrerede kliniske blik og evnen til at vurdere helhedsbilledet, som kendetegner den kliniske ekspert [25, 26]. Ideelt bør alle læger mestre både System 1 og System 2 og i særdeleshed være bevidste om, hvornår et skift fra System 1 til System 2 er indiceret, før kognitive bias fører til potentielt fatale fejldiagnoser [9, 26].
FPR tilpasset en klinisk kontekst (Figur 3) er et bud på en rammedannende System 2-analyseteknik, som især tænkes at være effektiv, når flere personer mobiliserer deres biomedicinske viden. Metoden kan introduceres allerede på medicinstudiets kandidatdel, hvor studerende typisk er med i en læsegruppe. I klinikken er morgen-, middags- og multidisciplinære konferencer tilsvarende oplagte situationer, hvor metoden kan anvendes. Undervejs kan den patientansvarlige kliniker dirigere analysen og holde visuel struktur og overblik over input og overvejelser vha. et whiteboard eller lignende.
Det er naturligvis afgørende, om FPR som beskrevet her er bedre end nuværende praksis. Det kunne undersøges i et randomiseret design, hvor man – efter at have taget højde for uddannelsestrin/erfaring – randomiserer læger til caseløsning med versus uden instruktion i FPR. Et relevant endepunkt er f.eks., om den korrekte diagnose bliver foreslået blandt differentialdiagnoserne, eller om en vigtig, særlig farlig, differentialdiagnose er overset.
Korrespondance Muhammad Sabbah. E-mail: muhammadsabbah.ms@gmail.com
Antaget 17. marts 2023
Publiceret på ugeskriftet.dk 24. april 2023
Interessekonflikter ingen. Forfatterens ICMJE-formular er tilgængelig sammen med artiklen på ugeskriftet.dk
Referencer findes i artiklen publiceret på ugeskriftet.dk
Artikelreference Ugeskr Læger 2023;185:V01230004
Muhammad Sabbah
Ugeskr Læger 2023;185:V01230004
Sound diagnostic reasoning is a defining characteristic of the expert clinician. The prevailing psychological model of reasoning describes two systems of thought: a fast, intuitive, but biased (System 1) and a rigorous, analytic, but slow (System 2). Clinicians use both systems during diagnostic reasoning but tend to lean toward a System 1-dominant approach as they get more experienced. This represents a potential source of diagnostic error, perhaps amenable to deliberate System 2 thinking. In this review, first principles reasoning is suggested as a method of System 2 thinking in a diagnostic context.