Intrakranielle ventrikulære shunts

Emma Tubæk Nielsen1, 2, Mathias Just Nortvig1, 2, 3, Sune Munthe2, Christian Bonde Pedersen1, 2, 3, Frantz Rom Poulsen1, 2, 3 & Mikkel Schou Andersen1, 2, 3
Fakta
Ventrikulær shuntbehandling er forbundet med risiko for komplikationer og dysfunktion, som kan være livstruende.
Shuntdysfunktion medfører især stillingsbetinget hovedpine, kvalme, opkastninger og/eller bevidsthedspåvirkning.
Kendskab til shuntdysfunktion er vigtig for rettidig udredning og behandling.
Drænage af cerebrospinalvæske (CSV) ved implantation af et slangesystem er en etableret, neurokirurgisk procedure til behandling af hydrocephalus. Første brug af en permanent shunt bleb foretaget af Mikulicz i 1891 på et barn med hydrocephalus. Første succesfulde ventrikuloperitoneale (VP) shunt fandt sted i 1908, men metoden fik først indpas i 1950’erne, hvor implantation af trykregulerede systemer blev introduceret. Siden hen er teknikken udvidet til at involvere hjertets forkammer, lungehinder og cerebrale vener [1].
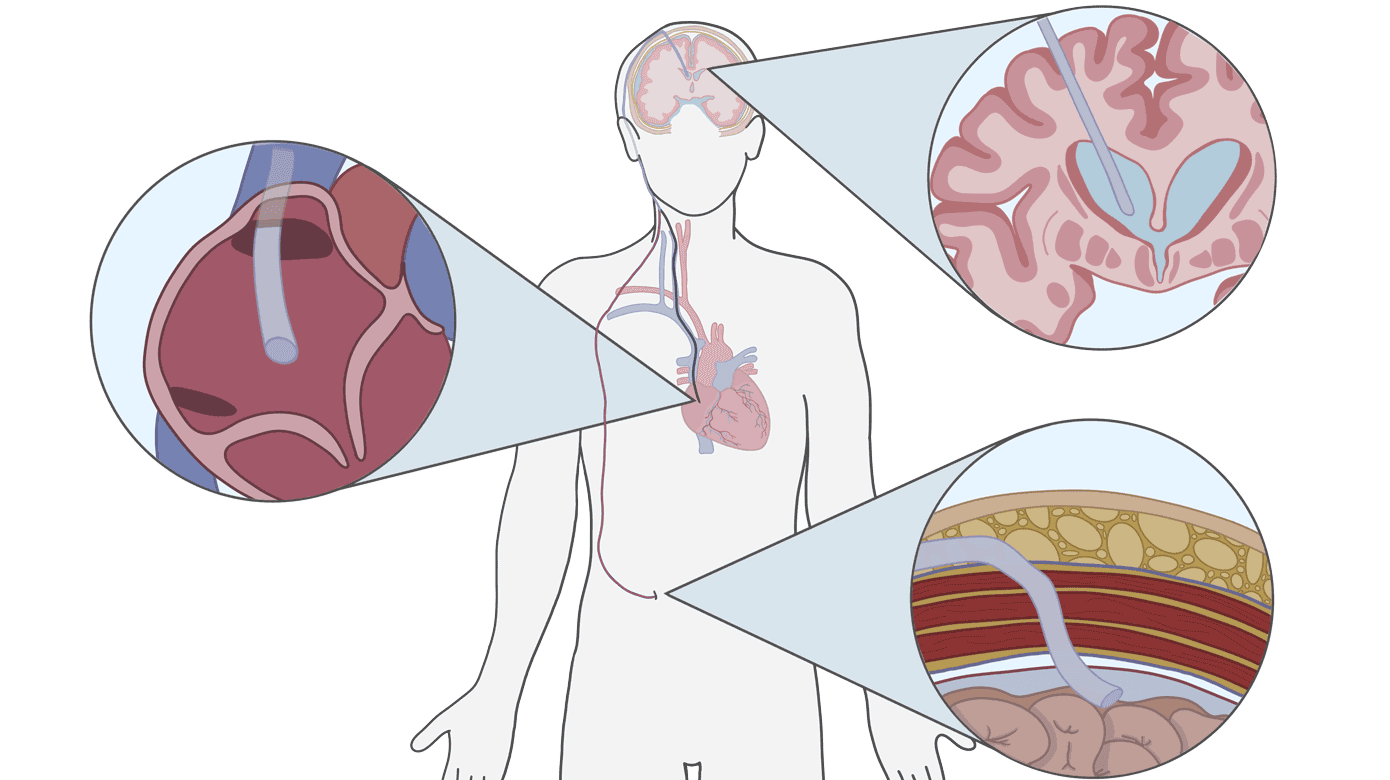
Grundprincippet bag shuntbehandling er normalisering af liquordynamikken ved drænage af CSV fra ventrikelsystemet til det systemiske kredsløb. Returneringen til kredsløbet er hyppigst via peritoneum ved en VP-shunt, eller via hjertets højre atrium ved en ventrikuloatrial shunt (Figur 1) [2, 3]. Alternativt kan CSV dræneres til galdeblæren eller til det pleurale rum, eller CSV kan ledes fra det lumbale subaraknoidalrum til peritoneum ved en lumboperitoneal shunt [4]. Shuntanlæggelse benyttes oftest til behandling af hydrocephalus, en lidelse karakteriseret af forstørrede ventrikler grundet uoverensstemmelse mellem CSV-produktion og CSV-absorption, og i begrænset omfang til idiopatisk, intrakraniel hypertension [5, 6].
Som alt implantationsmateriale kan shunts blive dysfungerende af mekaniske, funktionelle eller infektiøse årsager (se Tabel 1). Shuntdysfunktion og shuntinfektion kan være akutte, neurokirurgiske tilstande, og de kan medføre behov for shuntrevision [7, 8]. Risikoen for shuntdysfunktion er høj, og komplikationer hos shuntopererede patienter rammer 40% og 29% blandt henholdsvis børn og voksne [9]. Dette har også givet sig til udtryk ved et stigende antal ventrikulære shuntoperationer i Danmark i de sidste ti år. I 2022 registrerede Landspatientregisteret 917 shuntoperationer, hvoraf 461 var shuntrevisioner og shuntfjernelser. Denne artikel har til formål at give kendskab til ventrikulær shuntdysfunktion.
Hydrocephalus inddeles oftest på baggrund af ætiologien i kommunikerende og nonkommunikerende (obstruktiv) type samt en særlig subtype kaldet idiopatisk normaltrykshydrocephalus (iNPH) [5, 10].
Kommunikerende hydrocephalus er hyppigst forekommende og forårsages af CSV-overproduktion, inadækvat CSV-absorption eller en kombination heraf [11], hvoraf iNPH er en speciel subtype med særlige kliniske og radiologiske kendetegn [12]. Nonkommunikerende hydrocephalus skyldes intra- eller ekstraventrikulær obstruktion af det normalfysiologiske flow af CSV, f.eks. af tumor, cyste, membran eller medfødte malformationer [10].
Hydrocephalus hos spædbørn med åbne fontaneller kan præsentere sig med frembulende fontaneller, voksende hovedomfang, adfærdsændringer, irritabilitet, Macewens tegn (resonanslyd ved perkussion nær de kranielle suturer) og solnedgangsblik. Den posteriore fontanelle fusionerer inden for et par måneder efter fødslen, mens den anteriore fontanelle er åben i op til to år [13]. Hydrocephalus hos børn og voksne med lukkede fontaneller kan medføre hovedpine, opkastninger, bevidsthedspåvirkning, stasepapiller, synsforstyrrelser, gangpåvirkning og abducensparese. Klassisk er stillingsbetinget hovedpine, som forværres i liggende og lindres i oprejst stilling grundet tyngdekraftens påvirkning af det intrakranielle tryk (ICP) [6, 14].
Radiologisk billeddiagnostik inkluderer CT og MR-skanning af hjernen [5, 15]. CT af cerebrum har sin primære anvendelse til screening og akut udredning for hydrocephalus, særligt på grund af sin mere udbredte tilgængelighed [10]. MR-skanning af cerebrum er den foretrukne billeddiagnostiske undersøgelse til udredning af hydrocephalus, hvoraf fasekontrast-MR-skanning anvendes til visualisering af CSV-flowet i og omkring hjernen. Metoden muliggør mere detaljeret vurdering af forhold som akvæduktstenose (der ofte bør behandles med tredje ventrikulostomi og ikke shunt) samt radiologiske tegn til hydrocephalus: forstørrede ventrikler og temporalhorn, nedadbulende loft i tredje ventrikel, udtynding af corpus callosum og transependymal ekstravasion af CSV fra ventriklerne til hjernevævet [16].
En shunt består oftest af fire komponenter: proksimalt kateter, reservoir, ventil og distalt kateter. Forudgået af et borehul i kraniet indføres det proksimale kateter i en af de cerebrale lateralventrikler, mens det distale kateter indføres på lokationen for CSV-absorption. Shuntslangen løber altid subkutant fra kranie til indløbsstedet. Ventilens primære funktion er ensretning af flow væk fra de cerebrale ventrikler, og reservoirets beliggenhed oven på kraniet muliggør palpation og punktur [4, 17].
Valget af shunttype og ventiltype afhænger af patientens hydrocephalusætiologi, anatomiske og fysiologiske faktorer, alder, ventrikelstørrelser, tidligere prøvede shunttyper og ventiltyper samt klinikerens erfaringer.
Overordnet findes differentialtryksventiler og flowstyrede ventiler: forsimplet holder differentialtryksventiler samme tryk uanset flow, mens flowstyrede ventiler holder samme flow uanset tryk. Disse ventiler kan være ikkejusterbare eller justerbare. Differentialtryksventiler har et fastsat åbningstryk, hvor CSV dræneres, når differentialtrykket over ventilen overstiger ventilens åbningstryk. Differentialtrykket bestemmes af forskellen mellem trykket for shuntens proksimale ende, det vil sige ICP, og trykket for den distale ende, det hydrostatiske tryk og f.eks. det intraperitoneale tryk. Alle justerbare ventiler fungerer efter differentialtryksventilprincippet med et indstillet åbningstryk, der kan justeres efter behov for mere eller mindre drænage. Åbningstrykket kan reguleres af et eksternt, magnetisk værktøj, hvilket tillader noninvasiv justering.
Flowstyrede ventiler fungerer principielt ved, at flow ikke kan øges ud over en fastsat maksimal hastighed (volumen/tidsenhed), som modvirker sifoneffekten og beskytter mod overdrænage. Systemet kræver dog et vist intrakranielt tryk (f.eks. 9,6 mmHg – normalt ICP 0-15 mmHg for Orbis-Sigma-ventilen fra Integra), for at ventilen kan fungere flowstyret. Under det tryk fungerer ventilen som differentialtryksventil.
Liquordynamikken i shunten defineres ud fra det indstillede åbningstryk og den væskesøjle, som shunten drænerer over. Flowet øges derved i stående stilling grundet tillægget af vand under væskesøjlen. Denne effekt benævnes sifoneffekten, som bevirker, at CSV »suges« ned mod den distale kateterkavitet, indtil væsken opnår ligevægt mellem proksimal og distal kavitet. For at modvirke uhensigtmæssigt øget drænage i oprejst position kan en shunt med antisifon- eller antigravitetsmekanisme benyttes [3, 4].
Hydrocefalus udvalget i Dansk Neurokirurgisk Selskab udarbejdede i 2020 et shuntkatalog, der kort beskriver og begrunder anvendte ventiltyper i Danmark [18].
Hyppige årsager til shuntdysfunktion inddeles i tre kategorier: mekanisk, funktionel og infektiøs (Tabel 1) [19, 20].
Den hyppigste årsag til shuntdysfunktion er kateterobstruktion og udgør 30% [21]. Obstruktion kan forårsages af hjernebrok, glia- eller plexus choroideus-indvækst, tromber, infektion og proksimal eller distal kateterdisplacering.
Funktionel dysfunktion i form af over- og underdrænage giver uhensigtsmæssige ændringer af ICP. Underdrænage kan medføre akkumulering af CSV og korresponderende ICP-stigning, som giver hovedpine og kvalme i liggende stilling samt symptomlindring i oprejst stilling. Det gælder dog ikke patienter, hvor shunten er anlagt grundet normaltrykshydrocephalus. Overdrænage reducerer CSV-volumen og korresponderende fald i ICP. Symptomerne er mest udtalt i stående stilling, hvor sifoneffekten medfører yderligere ICP-fald. Ved overdrænage er der risiko for kroniske, subdurale hæmatomer, som i værste tilfælde er behandlingskrævende, samt slit ventricle-syndrom, hvor en eller flere ventrikler sammenklapper [6, 20].
Nyere studier rapporterer en shuntinfektionsrate på 5-12%, hvoraf 90% sker inden for seks måneder postoperativt, og infektion er anslået som årsag til 11% af shuntdysfunktioner [22].
Ved shuntkomplikation skal shunten ofte revideres. Shuntrevidering kan være operativ udskiftelse af en defekt shuntkomponent eller hele shuntforløbet. Revisionsraten efter første shuntoperation er omkring 40% [21, 23]. Børn har højere revisionsrate end voksne, særligt forårsaget af deres vækst, som medfører fysiologiske og anatomiske ændringer, hvilket betyder ændringer i shuntindstillinger og shunttype [24].
Anamnese skal – ud over det sædvanlige – indeholde symptomdebut samt symptomer på over- eller underdrænage, neuroinfektion og/eller forhøjet ICP. Hos børn undersøges hovedstørrelse og fontaneller, og forældre adspørges til adfærds- og trivselsændringer. Shuntdysfunktion kan give symptomer som hovedpine, kvalme, opkastninger, synsforstyrrelser, feber og adfærdsændringer. En VP-shunt kan give abdominale smerter, også uden dysfunktion, grundet dens intraperitoneale beliggenhed. Mere sjældent ses kranielle neuropatier og kramper.
I meget sjældne tilfælde kan bevidsthedstab indtræde, hvis hastig CSV-akkumulering medfører kraftig ICP-stigning. Disse tilfælde bør håndteres som anden cerebral katastrofe med intubation, hyperventilation og hypertont saltvand indtil hurtig kirurgisk intervention. Her tages øjeblikkelig kontakt til en neurokirurgisk afdeling [7, 25].
Objektivt inspiceres og palperes hele shuntens ekstrakranielle forløb, shuntreservoir, ventilen og shuntens distale placering. Har patienten en VP-shunt, gennempalperes abdomen, da shuntinfektion ofte giver peritonal ømhed og smerter. Et funktionelt shuntreservoir skal være komprimerbart efterfulgt af genopfyldning ved kompressionsophør. Er ventilen justerbar, foretages kontrol af det indstillede åbningstryk.
Radiologisk billeddiagnostik har en stor plads i shuntdysfunktionsudredning (Figur 2). Konventionel røntgenundersøgelse anvendes til billedfremstilling af shuntserier, hvor projektionerne anterior-posteriort plan og lateralplan kan fremstille shuntens forløb kranielt, torakalt og abdominalt. CT eller MR-skanning af cerebrum anvendes til vurdering af cerebral ventrikel-størrelse, subdurale ansamlinger (hygromer, hæmatomer) og udelukkelse af differentialdiagnoser. Uændrede intrakranielle forhold udelukker dog ikke shuntdysfunktion.
Hvis der er behov for en mere funktionel vurdering af shunten over en længere periode, kan der foretages kontinuerlig måling af ICP via shuntreservoir eller invasiv trykmåler. Hos særligt komplekse patienter kan telemetrisk måling af ICP overvejes, hvilket også muliggør, at patienterne selv kan måle ICP [26].
Ved mistanke om infektion eller proksimal shuntdysfunktion er det relevant at aftappe CSV fra shuntreservoiret i samråd med en neurokirurg. Proceduren omfatter palpation af shunten kranielt, afspritning af hud, indstik i reservoir med atraumatisk nål og tapning af CSV. CSV-prøver sendes til analyse for protein, glukose, leukocyttal og dyrkningsresistens. Er reservoiret ikke komprimerbart eller tapning ikke mulig, bør man overveje proksimal kateterdysfunktion.
En nyere metode til vurdering af shuntfunktion er nuklearmedicinsk undersøgelse af shuntflowet. Metoden er egnet til patienter, hvor billeddiagnostik viser uændrede shuntforhold, men klinisk præsentation eller ICP-måling rejser mistanke om shuntdysfunktion. Radioaktiv tracer-99mTc-DTPA (diethylen-triamin-penta-acetat) injiceres i shuntreservoiret og diffunderer i proksimal og distal kateterretning. Single photon-emissions-CT (SPECT)-CT-billeder tages hvert 15.-20. minut for at visualisere shuntens forløb [27].
Hjerneventrikelshunts er standardbehandling i en lang række tilfælde af hydrocephalus. Shuntdysfunktion er en hyppig komplikation hos shuntopererede patienter og kendetegnes især ved stillingsbetinget hovedpine, kvalme, eksplosive opkastninger og i mere sjældne tilfælde bevidsthedspåvirkning. Systematisk tilgang er vigtig for tidlig udredning af shuntdysfunktion. Patienter med hydrocephalus og udtalte symptomer eller mistanke om ICP-stigning kræver akut intervention og overflytning til en neurokirurgisk afdeling.
Korrespondance Emma Tubæk Nielsen. E-mail: emma.tubaek.nielsen@rsyd.dk
Antaget 30. januar 2024
Publiceret på ugeskriftet.dk 11. marts 2024
Interessekonflikter ingen. Forfatternes ICMJE-formularer er tilgængelige sammen med artiklen på ugeskriftet.dk
Referencer findes i artiklen publiceret på ugeskriftet.dk
Artikelreference Ugeskr Læger 2024;186:V08230515.
doi 10.61409/V08230515
Open Access under Creative Commons License CC BY-NC-ND 4.0
Permanent shunt diversion of cerebrospinal fluid away from the central nervous system is a widely recognized neurosurgical procedure. Still, patients with ventricular shunts are at substantial risk of shunt dysfunction, which includes complications like mechanical shunt failure, abnormal shunt drainage and infection. Early detection of shunt dysfunction is essential to proper and timely treatment, and acute shunt dysfunction might require immediate intervention. This review summarizes current and potential strategies for investigation of shunt dysfunction.