Recidiverende meningokoksygdom hos kvinde med mutation i C8B-genet

Ulrik Ørsø Andersen1, Jakob Thaning Bay2 & Lise Heilmann Jensen1
Lakunære immundefekter er karakteriseret ved en øget modtagelighed for en enkelt eller ganske få specifikke mikroorganismer, f.eks. pga. en defekt i komplementsystemet. Patienter med recidiverende meningokoksygdom (MS) bør derfor udredes for komplementdefekt (KD). Patienter med en terminal KD (C5-9) har op til 10.000 gange øget risiko for MS, og 40-50% vil opleve flere tilfælde, hvorfor korrekt diagnosticering og profylaktisk behandling er vigtig.
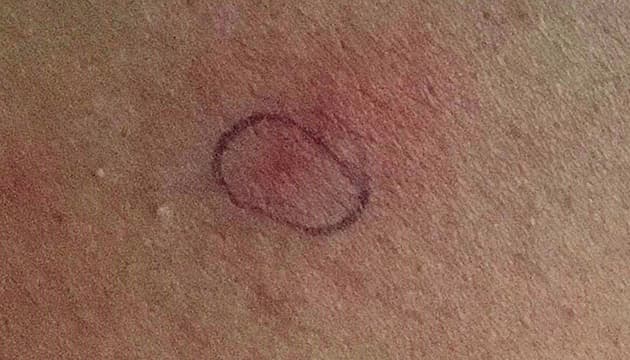
En 16-årig pige blev indlagt med et døgns feber, opkastninger, nakkesmerter og fotofobi. Ved indlæggelsen var hun klinisk stabil og ikke meningeal. Der blev fundet fire mikropetekkier (se Figur 1). CRP-koncentrationen var 99 mg/l. Spinalvæsken (CSV) var klar og uden pleocytose. Initial behandling for MS med ceftriaxon givet i.v. udløste en akut allergisk reaktion, og behandlingen blev omlagt til meropenem. Den følgende dag var patienten feberfri og upåvirket. Hun fik i.v.-antibiotika i tre dage og derefter peroral behandling med clindamycin og ciprofloxacin i en uge.
Bloddyrkning og CSV var uden vækst, og CSV var negativ for meningo- og pneumokokker ved PCR. Der var svag vækst af Neisseriameningitidis i svælget. Meningokokantistoftest (MAT) blev foretaget i den akutte fase og 22 dage efter indlæggelsen og bekræftede serologisk MS.
Som femårig havde patienten også et tilfælde med MS. Her blev hun indlagt med feber, petekkier og forhøjede infektionstal. CSV-analyse viste leukocytose, og mikrobiologisk udredning var negativ. Diagnosen blev bekræftet ved MAT med en titerstigning efter tre uger.
Pga. to meningokokinfektioner blev patienten udredt for KD. Komplementscreening viste total mangel af evnen til at danne det terminale komplementkompleks (TCC). Genetisk udredning påviste en homozygot mutation i genet for betakæden af komplementfaktor 8 (C8B) (c.1282C>T, p.Arg428Ter). Samme mutation er tidligere beskrevet værende patogen og associeret med invasiv MS [1]. Patientens søster blev undersøgt (hun var ikke kendt med tidligere MS), og man fandt den samme homozygote mutation i C8B. Analyse for C8 i blodet hos patienten og søsteren viste et kraftigt nedsat niveau. Forældrene er ikke beslægtede og er ikke udredt for KD.
Begge søskende blev efterfølgende vaccineret mod MS og skal ved feber indtage penicillin og henvende sig til hospital hurtigst muligt mhp. vurdering for invasiv sygdom.
Ved invasiv MS (N. meningitidis) kan de kliniske manifestationer variere fra feber til fulminant sygdom med døden til følge på få timer. Bekræftelse af diagnosen invasiv MS består i påvisning af meningokokker i blod, CSV eller andet materiale ved dyrkning og/eller PCR-teknik. I ca. 80% af alle tilfælde bekræftes diagnosen ved et positivt dyrkningsfund [2], og den hyppigst observerede serogruppe blandt patienter med KD er serogruppe Y [3]. I denne patientcase kunne der ikke dyrkes meningokokker i hverken blod eller CSV i de to sygdomsforløb. Patienten blev behandlet på den kliniske præsentation, som var forenelig med MS. I begge tilfælde blev MAT brugt til at bekræfte mistanken. I typiske tilfælde er MAT negativ i den akutte fase, men positiv i 2.-3. sygdomsuge, som det også var tilfældet her. MAT påviser komplementbindende meningokokantistoffer i serum og kan således bruges til at diagnosticere MS serologisk. Ved MAT anvender Statens Serum Institut en blanding af meningokokantigen udvundet fra et antal af de foregående 1-2 års modtagne isolater fra patienter med invasiv MS, idet det tilstræbes, at fordelingen af serogrupper i antigenblandingen svarer til fordelingen blandt disse patienter. Tidligere var serogruppe B og serogruppe C helt dominerende, men nu er serogruppe Y og serogruppe W blevet hyppigere, hvorfor disse også inkluderes.
N. meningitidis er den eneste mikroorganisme, hvor bekæmpelsen helt afhænger af et velfungerende komplementsystem, og den terminale lysering af mikroben er essentiel. I denne case blev der fundet en defekt i komplementproteinet C8, som medfører, at TCC ikke kan dannes [4]. Defekten disponerer til recidiverende MS, risiko for alvorlige infektioner og i værste fald død. Patienter med terminale KD’er har dog ofte et mildere sygdomsforløb af MS, som det også kunne ses hos denne patient [5], muligvis pga. mindre inflammation som følge af et ikke intakt komplementsystem.
Patienter med recidiverende MS eller med usædvanlige serogrupper bør udredes for KD, idet en hurtig diagnose er vigtig mhp. at forebygge gentagne infektioner. Påvisning af KD giver også mulighed for at screene asymptomatiske familiemedlemmer.
Korrespondance Ulrik Ørsø Andersen. E-mail: uan@regionsjaelland.dk
Antaget 12. april 2022
Publiceret på ugeskriftet.dk 6. juni 2022
Interessekonflikter ingen. Forfatternes ICMJE-formularer er tilgængelige sammen med artiklen på ugeskriftet.dk
Referencer findes i artiklen publiceret på ugeskriftet.dk
Artikelreference Ugeskr Læger 2022;184:V02220113
Ulrik Ørsø Andersen, Jakob Thaning Bay & Lise Heilmann Jensen
Ugeskr Læger 2022;184:V02220113
This is a case report of recurrent meningococcal infection in a young woman. She had no positive microbiological findings but was serologically diagnosed with the meningococcal antibody test. Investigation of the complement system showed no function of the terminal pathway. Further genetical analysis revealed a pathogen mutation in the C8B gene in the patient and her sister. They were both immunised with meningococcal vaccines. Complement deficiencies are rare but potentially fatal. Workup for complement deficiency is important for correct acute and prophylactic treatment.
Dellepiane RM, Dell'Era L, Pavesi P et al. Invasive meningococcal disease in three siblings with hereditary deficiency of the 8(th) component of complement: evidence for the importance of an early diagnosis. Orphanet J Rare Dis. 2016;11(1):64.
Weis N, Berthelsen L, Wachmann H et al. The meningococcal antibody test: how useful in the diagnosis of meningococcal disease? Epidemiol Infect. 2005;133(2):217-27.
Ladhani SN, Campbell H, Lucidarme J et al. Invasive meningococcal disease in patients with complement deficiencies: a case series (2008-2017). BMC Infect Dis. 2019;19(1):522.
Mayilyan KR. Complement genetics, deficiencies, and disease associations. Protein Cell. 2012;3(7):487-96.
Figueroa JE, Densen P. Infectious diseases associated with complement deficiencies. Clin Microbiol Rev. 1991;4(3):359-95.