Sent debuterende skizofreni

Camilla Krogh1, Janne-Elin Yttri1, Julie Nordgaard Frederiksen1, 2, Mads Gram Henriksen1, 3 & Annick Urfer-Parnas1, 2
Hovedbudskaber
De fleste patienter med skizofreni debuterer inden 25-årsalderen. Den tidlige debut blev allerede betonet med Emil Kraepelins begreb om dementia praecox, der netop betegner en tidligt indsættende form for afsind eller galskab [1]. Eugen Bleuler var kritisk overfor Kraepelins begreb om dementia praecox, og han omdøbte begrebet til skizofreni [2]. Kraepelin beskrev også en anden diagnose – parafreni – som betegnede en sent debuterende psykose, der i nogen grad lignede dementia praecox. Wilhelm Mayer-Gross foretog i 1921 en followupundersøgelse af Kraepelins patienter med parafreni, og her blev hovedparten af patienterne diagnosticeret med dementia praecox [3]. Dette studie foregriber den senere diskussion om, hvorvidt parafreni eller sent debuterende psykose udgør en selvstændig diagnostisk kategori eller en form for skizofreni [4].
I løbet af de seneste 40 år har et betydeligt fokus i både skizofreniforskning og klinikken været rettet mod tidlig opsporing og behandling af unge patienter i risiko for at udvikle skizofreni eller psykose. Dette fokus har muligvis samtidig medført en begrænset interesse for den subgruppe af patienter (ca. 20%), der først bliver diagnosticeret med skizofreni i en sen alder, typisk defineret som over 40 år. Manfred Bleuler kaldte denne subgruppe for »sent debuterende skizofreni« (SDS) [5]. Hos patienter med meget sen debut, typisk defineret som over 60 år, brugte man betegnelser som parafreni, involutiv psykose eller meget sen debut af skizofreni [6].
Litteraturen om SDS er præget af overlap af anvendte begreber (f.eks. SDS, parafreni, sen parafreni, og psykose af anden oprindelse) samt uklarhed om, fra hvilken alder »sen debut« bør defineres. Dette har gjort den tilgængelige forskning svær at sammenligne og drage konklusioner fra.
Formålet med denne artikel er at gennemgå de historiske og kliniske aspekter, der karakteriser patienter med SDS. Her følger vi Manfred Bleuler og definerer SDS som en tilstand, der debuterer hos patienter med skizofreni, efter at de er fyldt 40 år. Disse personer kan blive overset i klinikken, da sygdomspræsentationen – klinisk og socialt – ofte adskiller sig fra den, som man finder ved yngre debuterende patienter med skizofreni. Der er fortsat tvivl om, hvorvidt denne gruppe med sen debut skal være en selvstændig enhed eller klassificeres under skizofreni, som den findes i de nyeste internationale klassifikationer (DSM-5-TR og ICD-10) [7, 8].
Manfred Bleuler var den første til at anvende betegnelsen SDS i 1943. Han undersøgte sygdomsdebut hos 126 patienter over 40 år og beskrev SDS som en gruppe med psykose, der opfyldte de følgende tre kriterier [5]: 1) psykosen skal starte efter det 40. leveår, 2) symptomatologien må ikke adskille sig væsentligt fra tidligt debuterende skizofreni, og 3) der må hverken være anamnestisk syndrom eller andre tegn på organisk hjernesygdom
Manfred Bleuler fandt, at 15% af de patienter, der fik stillet en skizofrenidiagnose, havde første sygdomsudbrud i 40-60-årsalderen [9].
I DSM-III var det ikke muligt at stille en skizofrenidiagnose hos patienter over 45 år. I stedet blev diagnosen »paranoide tilstande« eller »atypisk psykose« brugt [6, 9]. I DSM-III-R blev det muligt at vælge »sen debut« som tillæg til skizofrenidiagnosen [9], mens aldersgrænsen på skizofreni helt blev fjernet i de efterfølgende udgaver af DSM. I modsætning til i DSM-III var der i ICD-9 ikke en aldersgrænse for skizofrenidiagnosen. Her indgik parafreni og sen parafreni under paranoid psykose, hvis kliniske billede ikke var domineret af de affektive eller disorganiserede symptomer [9]. I dag er der enighed om, at parafrenibegrebet bør undgås, og det er fjernet fra de diagnostiske systemer i ICD-10 og DSM-5-TR [7, 8]. Skønt ICD-10 og DSM-5-TR inkluderer SDS som en del af skizofrenidiagnosen [9], kunne der være en potentiel klinisk og forskningsmæssig fordel i at bevare SDS-kategorien for sig [10].
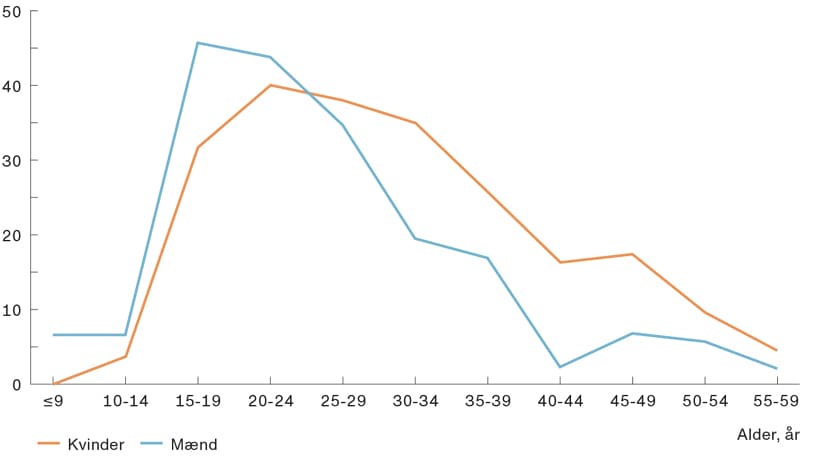
Det ser ud til, at der i mindre grad er familiær disposition for skizofreni og andre psykiske lidelser hos patienter med SDS [11, 12]. Livstidsrisikoen for udvikling af skizofreni er den samme for begge køn, men der ses en overvægt af kvinder med SDS [9, 13]. En hypotese til at forklare denne kønsmæssige forskel er, at østrogen har en beskeden beskyttende effekt for udvikling af skizofreni, og ved menopausen forsvinder denne effekt hos kvinderne [14, 15]. Der ses to aldersgrupper med øget incidens af nydiagnosticeret skizofreni hos kvinder: 20-29 år og 45-49 år [16]. Hos mænd ses derimod en høj incidens i aldersgruppen 15-24 år, derefter falder incidensen kontinuerligt [16] (Figur 1).
Patienterne med SDS klarer sig bedre socialt forud for diagnosen end patienterne med tidligere debuterende skizofreni (TDS) (før det 40. leveår). Dette vurderes på færdiggørelse og niveau af uddannelse, tilknytning til arbejdsmarkedet og økonomisk selvstændighed. Patienter med SDS har oftere været gift eller er i ægteskab og har flere børn [13, 16, 17]. Dog findes der også studier, der viser, at patienter med SDS før sygdommen har haft færre venner end patienter med TDS [12, 18], og at patienter med SDS har levet et mere isoleret liv [19, 20]. Patienternes sociale profil er således ikke entydig.
Et tiårsfollowupstudie viste, at efter sygdomsdebuten faldt andelen af patienter med SDS, som var selvforsørgende, fra 84% til 29% [16]. Imidlertid var andelen af selvforsørgende patienterne med TSD relativt uændret efter ti år. Forskellen mellem de to grupper blev fortolket således, at patienter med SDS havde opnået flere sociale kompetencer og var mere modstandsdygtige, og når de så blev syge, faldt funktionsevnen samt kompetenceniveauet. Dog fandt man i studiet også, at patienter med SDS formåede at holde et højere funktionsniveau end patienterne med TDS efter symptomdebut [16]. Endelig har et studie vist, at patienter med SDS har et mindre forbrug af både cannabis og amfetamin end patienter med TDS [13].
SYMPTOMER
Mayer-Gross et al beskriver, at nogle patienter med SDS kan skjule deres psykotiske oplevelser i årevis, og at de kan formå at klare job og sociale relationer. Pludselig kan en belastende situation medføre, at de ikke længere kan skjule psykosen, som så bryder tydeligt frem [21]. Mayer-Gross et al beskriver en succesfuld direktør, der pludselig fortalte sin kompagnon, at han var en illegitim søn af kongelige forældre, og at han havde overlevet flere forgiftningsforsøg de seneste mange år. Nogle patienter med SDS kan have været psykotiske i årevis, før de kommer i kontakt med psykiatrien. Det kan tænkes, at det psykopatologiske fænomen dobbelt bogholderi i nogen grad kan forklare dette. Dobbelt bogholderi betegner en evne til at leve og navigere samtidigt i to forskellige verdener – den fælles sociale verden og en privat-solipsistisk verden (som kan blive psykotisk) [22, 23]. Patienter med skizofreni kan således til tider adskille deres psykotiske oplevelser fra de oplevelser, der vedrører den fælles sociale verden. Dog kan det dobbelte bogholderi bryde sammen, hvorved patienterne ikke længere kan skelne disse verdener fra hinanden, og det er måske her, de kommer i kontakt med psykiatrien [23].
Vedrørende den præmorbide fase peger nogle studier i retning af paranoide og skizotypiske personlighedstræk, der kunne tolkes som en personlighedsforstyrrelse [10, 12], mens man i andre ikke har fundet påfaldende personlighedstræk før sygdomsudbrud [21]. Hos nogle patienter synes de psykotiske oplevelser at være en forlængelse af et tema, som patienten har været optaget af gennem dele af sit liv, f.eks. retfærdighed eller en religiøs interesse, som så får en psykotisk dimension.
På trods af et tilsyneladende upåfaldende præmorbidt funktionsniveau viser mange patienter med SDS sig alligevel ved nærmere undersøgelser at have haft en vis grad af sociale vanskeligheder gennem livet, som de dog har kunnet håndtere. En mulig forklaring herpå er, at patienter med SDS, som har været velfungerende og uden tegn på psykisk sygdom, alligevel har haft en sårbarhed for at udvikle psykotiske symptomer på baggrund af belastning, somatisk sygdom, eksistentielle forandringer eller begivenheder, som udløser et betydeligt følelsesmæssigt respons, såsom fyring fra job, skilsmisse eller migration [13]. En anden hypotese er en snigende udvikling af skizofreni over mange år.
Der er diskussion om, hvorvidt patienter med SDS har haft symptomer gennem mange år (potentielt hele livet) men først bliver diagnosticeret efter mange års uidentificeret sygdom, eller om symptomerne først begynder at vise sig pludseligt og tydeligt i en sen alder efter et helt liv uden tegn på skizofrenispektrumslidelse [6]. Det åbner et konceptuelt spørgsmål om sygdomsdebut, som man i klinikken ofte daterer til første kontakt med det psykiatriske system.
Symptombilledet hos patienter med SDS er ofte domineret af vrangforestillinger af persekutorisk karakter og hørehallucinationer [16, 24]. Deres sygdomsbillede er ofte mindre disorganiseret [6, 25], og de har typisk færre formelle tankeforstyrrelser [19, 26] og affektforstyrrelser [10, 25] end patienter med TDS. Patienterne med SDS kan således tænkes at tilhøre gruppen med den paranoide subtype af skizofreni [21].
Op til sygdomsdebut har patienter med SDS ofte ikke udtalte negative symptomer [17, 26]. Der findes dog også studier, hvori man ikke finder signifikante forskelle i graden af negative og positive symptomer, når man sammenligner patienter med SDS og TDS [10, 16, 17, 26].
Der ses en svækkelse af kognitive funktioner hos patienter med skizofreni afhængigt af alderen ved symptomdebut. Sammenlignet med alderssvarende raske kontrolpersoner findes der dog ikke forskel mellem patienter med TDS og SDS [27]. Dog tyder nogle studier på, at patienter med SDS klarer sig bedre end patienter med TDS, når det handler om indlæring, arbejdshukommelse, abstraktion og forestillingsevne [27, 28]. Til forskel fra patienter med TDS ser det ikke ud til, at den semantiske hukommelse afficeres hos patienter med SDS, hvilket måske indikerer, at SDS ikke er et forstadie til demens, som nogle har hævdet [28].
Det er desuden uklart, hvorvidt patienterne med SDS adskiller sig neurobiologisk fra patienter med tidligere debut [28].
Patienter med SDS har efter sygdomsdebut kortere indlæggelser samt færre genindlæggelser end patienter med TDS [15, 18, 29]. En faktor, som måske kan bidrage til det mildere forløb hos patienter med SDS, kan være bedre effekt og dermed mindre doser af antipsykotika end for patienter med TDS [10, 17, 30]. Litteraturen tyder på, at patienter med SDS hurtigere bliver symptomfrie og stabile i deres sygdomsforløb, hvilket bidrager til en god prognose efter den første indlæggelse [15, 17, 19].
Der er fortsat en række uafklarede kliniske og biologiske aspekter vedrørende SDS, og litteraturen er præget af inkonsistente fund. Måske kan en etablering af SDS som en selvstændig diagnostisk kategori føre til mere forskning og et øget klinisk fokus på denne i nogen grad uensartede gruppe af patienter. Der mangler i dag mere detaljeret viden om disse patienters præmorbide og prodromale faser. Beskytter deres højere præmorbide funktionsniveau og personlighedstræk i mange år mod udviklingen af skizofreni? Har disse patienter en prodromal fase, hvor sygdommen længe holdes i skak af autoprotektive copingmekanismer, indtil de på et tidspunkt får behov for psykiatrisk hjælp? Eller alternativt: Opstår sygdommen mere pludseligt? Er der antropologiske-psykologiske eller biologiske faktorer, der bidrager til sygdomsudvikling? En afklaring af disse spørgsmål kan bidrage med vigtig viden om variationen i udvikling af skizofreni og sygdomsforløb. Ligeledes kan kendskab til potentielt anvendte copingstrategier hos patienter med SDS have terapeutisk værdi i recoveryprocessen for såvel patienter med SDS som TDS.
Korrespondance Camilla Krogh. E-mail: camillakrogh06@regionh.dk
Antaget 6. januar 2023
Publiceret på ugeskriftet.dk 13. februar 2023
Interessekonflikter Der er anført potentielle interessekonflikter. Forfatternes ICMJE-formularer er tilgængelige sammen med artiklen på ugeskriftet.dk
Referencer findes i artiklen publiceret på ugeskriftet.dk
Artikelreference Ugeskr Læger 2023;185:V10220591
Camilla Krogh, Janne-Elin Yttri, Julie Nordgaard Frederiksen, Mads Gram Henriksen & Annick Urfer-Parnas
Ugeskr Læger 2023;185:V10220591
Patients with late-onset schizophrenia form a subgroup of schizophrenia that to some extent differs from the typical Gestalt of schizophrenia. Therefore, some of these patients may be overlooked in the clinic. This review describes the characteristics of the late-onset subgroup: Overweight of women, higher education, has been or is still married, and with more children than patients with early onset schizophrenia. The symptomatology of the subgroup is characterised by persecutory delusions and auditory hallucination. Knowledge of this subgroup of patients may lead to attention in the clinic and hopefully have therapeutic value in the recovery process for the patients.