Visceral leishmaniasis diagnosticeret ved mikrobiom 16S/18S-test

Kaziwa B. Rasoul1, Henrik Vedel Nielsen2, Anne-Luise Thorsteinsson1 & Anders Porskrog3
Visceral leishmaniasis i de nordlige dele af Europa er et sjældent fund og kan være svært at diagnosticere. Leishmaniasis findes almindeligvis i de tropiske og subtropiske dele af verden, herunder middelhavslandene. Den forekommer som importeret sygdom i Nordeuropa, men er endemisk i store dele af Sydeuropa f.eks. Spanien og Italien, hvor mange danskere tager på turistrejser. Leishmania-parasitten er vektorbåren og smitter via sandfluer [1].
I lighed med tuberkulose kan leishmaniasis forblive latent efter primærinfektion.
Mikrobiom 16S/18S er baseret på next-generation sequencing (NGS)- teknologien i kombination med automatisk artsidentifikation via BION-programmet for både bakterier, svampe og parasitter. Testen er baseret på Illumina MiSeq NGS-sekventering og tager ca. en uge at analysere [2]. Prøvematerialet kan være blod, cerebrospinalvæske, vævsbiopsier eller andre kropsvæsker såsom ascites, urin og pleuravæske [3].
Immunsupprimerede patienter, herunder især de hæmatologiske og onkologiske, bliver ofte indlagt under deres behandlinger, da de er modtagelige over for opportunistiske infektioner.
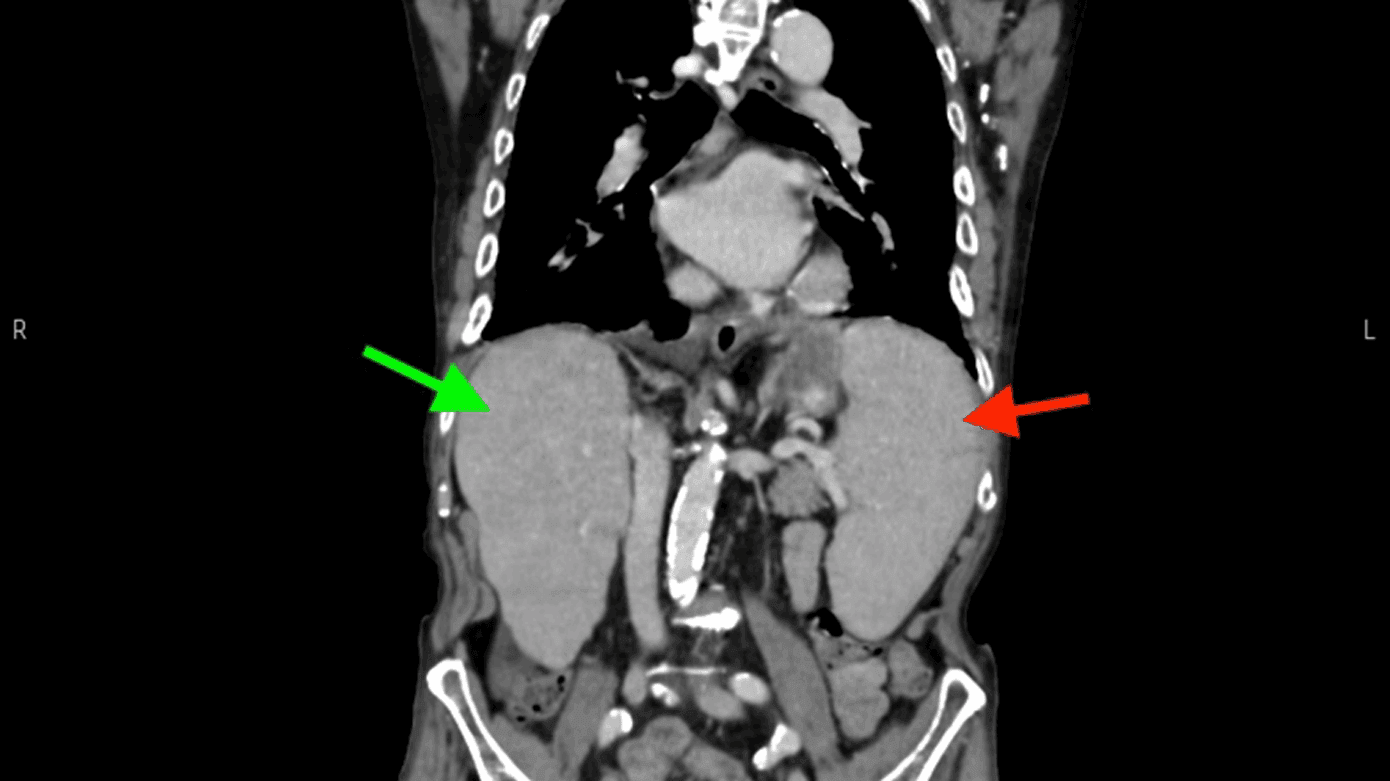
En 86-årig etnisk dansk mand diagnosticeret med letkæde lambda myelomatose i 2. linjebehandling med kemoterapi blev fulgt i hæmatologisk regi siden 2019. I løbet af et år havde patienten ca. ti indlæggelser med nedsat almen tilstand, recidiverende feber og forhøjede infektionsparametre uden fokus. Patienten opnåede kun kortvarig lindring på intravenøs antibiotisk behandling førend næste indlæggelse. En CT under en af indlæggelserne viste både hepato- og splenomegali (Figur 1). Blodprøver viste pancytopeni med hæmoglobin < 7,0 mmol/l, leukocytter < 2,0 mia./l og trombocytter < 60 mia./l, som initialt blev tilskrevet enten nytilkommet myelodysplastisk syndrom (MDS) eller progressiv myelomatose.
Patienten blev grundigt udredt over længere tid uden nye fund. På den baggrund blev det besluttet at indstille den aktive kemobehandling og overgå til palliativ steroidbehandling, da man mistænkte behandlingssvigt. Ved en knoglemarvsbiopsikontrol fandt man dog ikke progressiv sygdom og ej heller tegn til MDS.
Grundet langvarig uafklaret feber blev der udbedt tilsyn fra infektionsmedicinsk afdeling. Ekspositioner viste en ekstensiv rejsehistorik i både Asien, Sydamerika og Sydspanien. Der anbefaledes supplerende mikrobiom 16S/18S på ethylendiamintetraacetat (EDTA)-blod. Denne var positiv for Leishmania. Sekvensering af internal transcribed spacer (ITS)-genet identificerede L. donovani/infantum-komplekset, hvilket bekræftede diagnosen visceral leishmaniasis. Dette forklarede patientens hepato- og splenomegali samt pancytopeni. Den seneste knoglemarvsbiopsi blev reevalueret af patologerne, men uden fund af amastigoter, som kan ses ved leishmaniasis. Patienten opstartede intravenøs liposomal amphotericin B og mærkede klar bedring allerede efter første behandling. Kort efter anden dosis ophørte feberen, og patientens biokemi bedredes. Hæmatologisk set var myelomatosen under kontrol, og patienten blev sat i behandlingsfri observation efter udtrapning af steroid.
At optage en grundig anamnese om ekspositioner, herunder om der flere år tidligere har været mulige ekspositioner for latente infektioner er yderst vigtig. Patienten her havde både rejst før myelomatosediagnosen og under kemoterapien. Latente infektioner kan reaktivere i forbindelse med immunsuppression.
Kasuistikken understreger de muligheder og fordele, der kan være ved brug af en bred »unbiased«-analyse som mikrobiom 16S/18S, når der ikke kan findes en oplagt årsag til infektioner ved grundig undersøgelse. Metoden kan identificere mere end 50.000 prokaryote og eukaryote arter. Derfor vil risikoen for falsk-positive resultater også være høj, og positive resultater kan være ret svære at tolke. 16S/18S er mindre sensitiv end den specifikke Leishmania real-time PCR til at diagnosticere Leishmania-species, hvorfor det anbefales evt. at benytte testen som et supplement til mere specifikke analyser.
I kommende år kan det forventes at se flere non-hiv-relaterede tilfælde af visceral leishmaniasis grundet et stigende antal patienter, der får immunmodulerende medicin. Da flere af patienterne har øget rejseaktivitet, må der også forventes flere tilfælde i nonendemiske lande [4, 5]. Smitte med Leishmania kan ske selv ved korte rejser til almindelige turistmål i Sydeuropa, og sygdomsmanifestation kan ses flere år senere. Det er også vigtigt at have for øje, at disse mere eksotiske sygdomme kan imitere hæmatologiske sygdomme grundet f.eks. pancytopenier.
Korrespondance Kaziwa B. Rasoul. E-mail: kaziras94@gmail.com
Antaget 13. februar 2025
Publiceret på ugeskriftet.dk 14. april 2025
Interessekonflikter ingen. Forfatternes ICMJE-formularer er tilgængelige sammen med artiklen på ugeskriftet.dk
Referencer findes i artiklen publiceret på ugeskriftet.dk
Artikelreference Ugeskr Læger 2025;187:V08240522.
doi 10.61409/V08240552
Open Access under Creative Commons License CC BY-NC-ND 4.0
Visceral leishmaniasis in northern parts of Europe is rare and can be difficult to diagnose. The microbiome 16S/18S-test is based on next-generation sequencing (NGS)-technology and a software program able to species annotate most types of bacteria, fungi, and parasites. We present a case of an 86-year-old male born in Denmark with multiple myeloma diagnosed with visceral leishmaniasis via the 16S/18S metabarcode test. This case highlights the potential of the test and the importance of obtaining a thorough travel anamnesis, as immunocompromised patients are susceptible to opportunistic infections.